Pohľad na kardiorenálny syndróm
A view on the cardiorenal syndrome
The cardiorenal syndrome was defined for the first time in the USA in 2004 (by workers of NHLBI – National Heart, Lung and Blood Institute) as follows: it is the condition of an organism affected by heart failure (HF), where the treatment of HF is limited in intensity due to impaired renal functions of the patient [1]. Today the incidence of HF is on a scale of an epidemic and it has reached approx. 2% of our populations in Europe, and approx. 10% of the people aged ≥ 65 and with advancing age it continues to rise exponentially (approx. 20% of people aged ≥ 80–85 [2,3]. The renal function disorder (dysfunction or insufficiency) is very frequent in individuals with HF, in part also in relation to the increasing life expectancy of citizens [4]. Regarding the acute HF the incidence of renal insufficiency reaches approx. 30–35% and it doubles for the chronic HF, approx. 60–70% [3,4]. The mutual incidence of HF and renal failure significantly worsens patients‘ prognosis, i.s. their morbidity, mortality and rehospitalizations as well as life quality [4,5]. The patients with chronic HF suffer from renal insufficiency (RI) more often than those with CRS, however without heart failure [4]. The incidence of HF correlates with the decrease in glomerular filtration in patients. RI is a strong and independent risk factor of mortality in patients with HF [5,6,7]. Our experience of the cardiorenal syndrome: In the period of 10th–12th months/2008 we analyzed the admissions of patients for emergency care at our establishment: (a) 1052 individuals were examined, (b) 302 were admitted for treatment, (c) the largest number of the admitted (45 individuals) suffered acute HF. 18 individuals (40 % among those admitted for the acute HF) had diabetes. Of the patients admitted all diabetic patients had chronic renal insufficiency (at average age of 77 years) while its presence was found in 3/4 nondiabetic patients (at average age of 80 years.) The patients with diabetes were more seriously ill than those without diabetes. The incidence of renal insufficiency/failure in people with HF, mainly chronic, is frequent. It will surely increase in future due to improvements in the treatment of CRS and increasing life expectancy. Extending of the knowledge about the syndrome pathophysiology is important for us to be able to improve the prevention and treatment of this complex disease.
Key words:
heart failure – renal insufficiency – diabetes – treatment – prognosis
Authors:
Ján Murín; Miroslav Pernický; Marta Filková
Authors‘ workplace:
I. interná klinika LF UK a UN, Bratislava, Nemocnica Staré Mesto, prednostka doc. MUDr. Soňa Kiňová, PhD.
Published in:
Forum Diab 2015; 4(3): 177-180
Category:
Main Theme: Review
Overview
Kardiorenálny syndróm definovali prvýkrát v roku 2004 v USA pracovníci NHLBI (National Heart, Lung and Blood Institute) nasledovne: je to stav organizmu pacienta so srdcovým zlyhávaním (SZ), u ktorého je liečba SZ vo svojej intenzite obmedzovaná zhoršením obličkových funkcií [1]. Výskyt SZ má dnes epidemický rozmer a predstavuje asi 2 % populácie v Európe, u osôb ≥ 65 rokov je to asi 10 %, v ďalších rokoch ich podiel ešte exponenciálne stúpa (asi 20 % u osôb ≥ 80–85 rokov) [2,3]. Renálna funkčná porucha (dysfunkcia či insuficiencia) je u osôb so SZ veľmi častá, sčasti tiež súvisí s narastaním priemernej dĺžky prežívania občanov [4]. U akútneho SZ je výskyt renálnej insuficiencie asi 30–35 % a u chronického SZ dvakrát viac, asi 60–70 % [3,4]. Vzájomný výskyt srdcového a renálneho zlyhávania významne zhoršuje prognózu chorých, teda jeho morbiditu, mortalitu a rehospitalizácie, i kvalitu života [4,5]. U chorých s chronickým SZ býva renálna insuficiencia (RI) častejšie ako osôb s kardiovaskulárnym ochorením, ale bez srdcového zlyhávania [4]. Výskyt SZ koreluje s poklesom glomerulárnej filtrácie chorých. RI je silným a nezávislým rizikovým faktorom mortality u chorých so SZ [5,6,7]. V období X–XII/2008 sme analyzovali príjmy pacientov v pohotovostných službách na naše pracovisko: vyšetrených bolo 1052 chorých, 302 bolo prijatých, najviac prijatých (45 osôb) bolo pre akútne SZ. 18 osôb (40 % medzi osobami prijatými pre akútne SZ) malo diabetes. Prítomnosť chronickej renálnej insuficiencie mali všetci diabetici (priemerný vek 77 rokov) a 75 % nediabetikov (priemerný vek 80 rokov). Pacienti s diabetom boli ťažšie chorí ako nediabetici. Výskyt renálnej insuficiencie/zlyhania je u osôb so SZ, hlavne chronickým, častý. Lepšou KV-liečbou a predlžovaním veku bude v budúcnosti výskyt RI iste stúpať. Poznanie patofyziológie syndrómu je dôležité, aby sme zlepšili prevenciu i liečbu tohto zložitého ochorenia.
Kľúčové slová:
diabetes – liečba – prognóza – renálna insuficiencia – srdcové zlyhávanie
Úvod
Kardiorenálny syndróm definovali prvýkrát v roku 2004 v USA pracovníci NHLBI (National Heart, Lung and Blood Institute) nasledovne: je to stav organizmu pacienta so srdcovým zlyhávaním (SZ), u ktorého je liečba SZ vo svojej intenzite obmedzovaná zhoršením obličkových funkcií. Následne skupina expertov z Talianska v roku 2008 vytvorila patofyziologickú definíciu tohoto syndrómu[1]. Táto definícia zohľadňuje vzájomný a obojstranný vplyv „interakcií zlyhávania srdca i obličiek“, pri ktorých dysfunkcia jedného z orgánov vyvoláva dysfunkciu druhého orgánu – hlavne prostredníctvom podobných hemodynamických, neurohormonálnych, imunologických aj biochemických zmien [1].
Epidemiológia syndrómu
Výskyt SZ má dnes epidemický rozmer a predstavuje asi 2 % populácie v Európe, u osôb ≥ 65 rokov je to asi 10 %, v ďalších rokoch ich podiel ešte exponenciálne stúpa (asi 20 % u osôb ≥ 80–85 rokov). Sú dve hlavné príčiny epidemického výskytu SZ – predlžovanie veku občanov vo vyspelých krajinách a dnes lepšia liečba väčšiny kardiovaskulárnych ochorení, na ktoré v minulosti mnohí chorí zomierali (infarkt myokardu, cievne mozgové príhody, revaskularizačné operácie, operácie chlopní a pod), ale dnes oveľa menej [2,3].
Renálna funkčná porucha (dysfunkcia či insuficiencia) je u osôb so SZ veľmi častá, sčasti tiež súvisí s narastaním priemernej dĺžky prežívania občanov. U akútneho SZ je výskyt renálnej insuficiencie asi 30–35 % a u chronického SZ dvakrát viac, asi 60–70 %. Vzájomný výskyt SZ a renálneho zlyhávania významne zhoršuje prognózu chorých, teda jeho morbiditu, mortalitu a rehospitalizácie, i kvalitu života [4,5].
Prognostický vplyv renálnej insuficiencie u SZ
U chorých s chronickým SZ býva renálna insuficiencia (RI) častejšie ako u KV chorých, ale bez srdcového zlyhávania [4]. Výskyt SZ koreluje s poklesom glomerulárnej filtrácie chorých. RI je silným a nezávislým rizikovým faktorom mortality u chorých so SZ [5,6,7]. Hillege et al analyzovali dlhodobo súbor asi 1 900 pacientov s kardiorenálnym syndrómom (osoby v NYHA triedach III a IV, so systolickým SZ a s ejekčnou frakciou ≤ 35 %, u ktorých vstupná priemerná glomerulárna filtrácia, kalkulovaná podľa Cockroft-Gaulta, bola 63 ml/min): hlavným prediktorom mortality bola u chorých vstupná glomerulárna filtrácia, až potom nasledovala hodnota NYHA triedy a úspešné pre prognózu chorých bolo podávanie ACE-inhibítorov. Chorí s najnižšou glomerulárnou filtráciou (eGF – kvartil s eGF < 44 ml/min) mali trojnásobne vyššie riziko mortality ako osoby v „najlepšom kvartile eGF“ (> 76 ml/min.), teda relatívne riziko tu bolo RR -2,85 (štatisticky významné) [5]. Aj ejekčná frakcia ľavej komory nebola štatisticky významná ako prognostický ukazovateľ. To poukazuje na väčšiu prognostickú výpoveď eGF, než je funkcia ľavej komory (ejekčná frakcia) [5].
U chorých v terminálnej fáze renálneho zlyhávania je KV mortalita dominantná a dosahuje ≥ 50 % prípadov. U chronickej renálnej insuficiencie je vaskulárne úmrtie asi 15 až 20-násobne vyššie než u rovesníkov bez renálneho zlyhávania. A mnohí chorí s renálnou insuficienciou trpia aj SZ súčasne [8]. Asi 75 % chorých s terminálnym renálnym zlyhávaním má hypertrofiu myokardu (často veľmi veľkú) a asi 40 % z nich trpí klinickou formou ischemickej choroby srdca [6,8,9].
Patofyziologické mechanizmy u kardiorenálneho syndrómu
Za hlavný faktor zhoršovania renálnych funkcií sa tradične uvádza nedostatočný prietok obličkou pri zníženom srdcovom minútovom výdaji (SZ). Asi sa tu uplatňuje aktivácia systému renín-angiotenzín-aldosterón (RAAS), a to uvoľnením renínu v obličke, ak je táto ischemizovaná. Ale mnohé klinické sledovania preukázali, že zvýšenie srdcového výdaja nevedie vždy k zlepšeniu renálnych funkcií [10,11].
A tak sa hľadali i alternatívne patofyziologické mechanizmy syndrómu, vysvetľujúce zlú prognózu chorých. U ťažších foriem SZ býva výrazne zvýšený centrálny žilný tlak. Isté práce preukázali, že nárast výšky centrálneho žilného tlaku asociuje s progresívnym poklesom obličkových funkcií u SZ. Vtedy klesá postupne diuréza. U asi 50 % chorých nachádzame vzostup centrálneho žilného tlaku, ak ide o pacientov s akútnou dekompenzáciou chronického SZ (s ejekčnou frakciou < 20 %), teda ak ide o ťažké systolické SZ [12,13].
Aj hyperaktivácia sympatického nerového systému je u tohto syndrómu významná: pre pokles renálneho prietoku v dôsledku vazokonstrikcie, pre uvoľňovanie katecholamínov do cirkulácie, pre zhoršené vylučovanie katecholamínov močom (pri renálnej insuficiencii). Isté práce preukázali, že „renálny obrat noradrenalínu!“ je silným rizikovým faktorom mortality u osôb s pokročilým chronickým SZ (čakajúcich na transplantáciu srdca) [14].
Problematika vzťahu aktivácie RAAS k mortalite i morbidite u SZ, ale i u renálneho zlyhávania (a tiež u oboch zlyhávaní spoločne) je preštudovaná a dobre známa. Inhibícia RAAS (ACE inhibítory, aldosterónové inihibítory) sú tu priaznivé: znižujú tonus sympatiku, zlepšujú endotelovú funkciu, bránia (spomaľujú) vývoju myokardiálnej fibrózy. Spomínané priaznivé efekty boli overené vo viacerých klinických štúdiách [15].
Zdá sa, že aj nárast oxidatívneho stresu má u kardio-renálneho syndrómu významné postavenie [16].
Aj anémia patrí k rizikovým faktorom tohto syndrómu. Anémia u chronického SZ zvyšuje mortalitu, predlžuje dobu hospitalizácií a zvyšuje riziko rehospitalizácií. Zdá sa, že podobne je to aj u RI, hoci tu môže byť aj len prejavom ochorenia obličky. U chorých s kardiorenálnym syndrómom býva anémia spojená s nedostatočnou produkciou erytropoietínu, no a erytropoietín – zdá sa – bráni apoptóze buniek renálneho parenchýmu, znižuje oxidatívny stres a asi má aj kardioprotektívne pôsobenie.
Iné faktory:
- úloha systému arginín-vazopresín (reguluje homeostázu vody a soli) nie je vyjasnená; antagonisty receptora (V1) pre vazopresín vedia zvýšiť diurézu a korigovať hyponátriémiu, ale štúdie nepreukázali benefit na KV-príhody
- adenozín nie je dostatočne prebádaný u kardiorenálneho syndrómu; antagonisty receptora adenozínu (A1) viedli k zvýšeniu glomerulárnej filtrácie (asi o 30 %), ale nebol opäť benefit na klinické príhody
- veľký výskum je v oblasti liečiv, ktoré stimulujú cGMP (zlepšuje to diurézu), ale tu nemáme ešte jasné klinické výstupy [18,19]
Naše skúsenosti s kardiorenálnym syndrómom
V období X–XII/2008 sme analyzovali príjmy pacientov v pohotovostných službách na naše pracovisko:
- vyšetrených bolo 1 052 chorých
- 302 bolo prijatých
- najviac prijatých (45 osôb) bolo pre akútne SZ; 18 osôb (40 % medzi osobami prijatými pre akútne SZ) malo diabetes
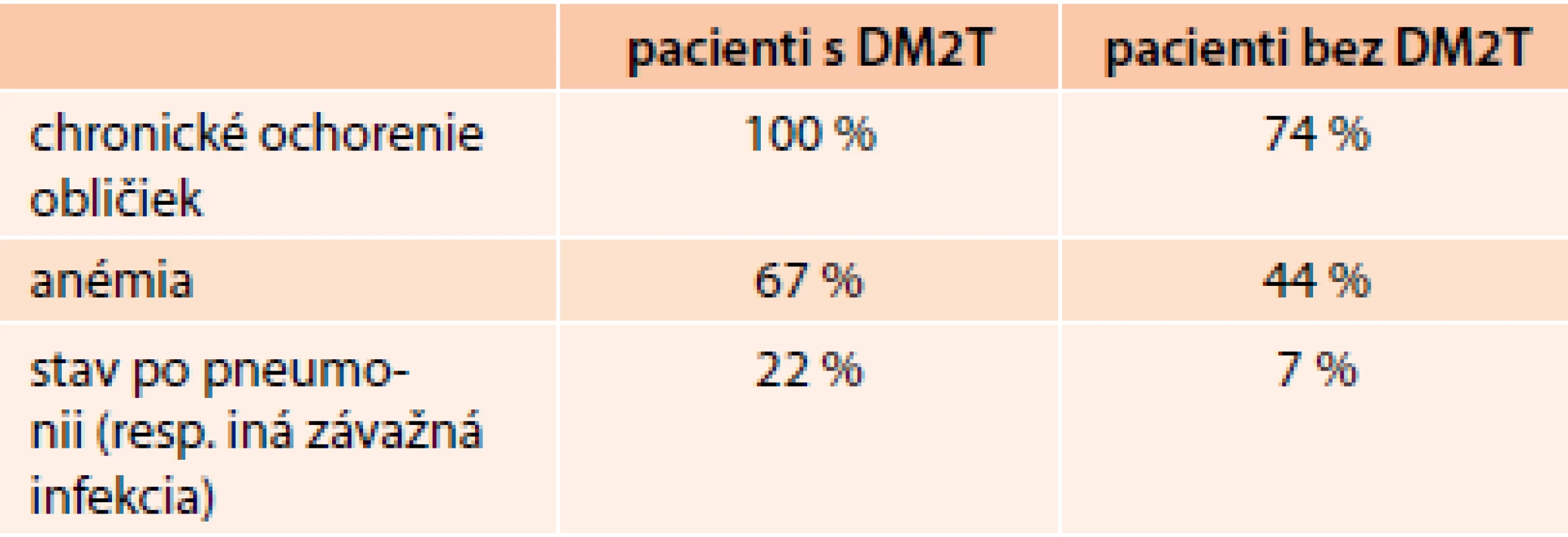
- komorbidity (ne/kardiovaskulárne) u prijatých s akútnym SZ uvádzajú tab. 1,2
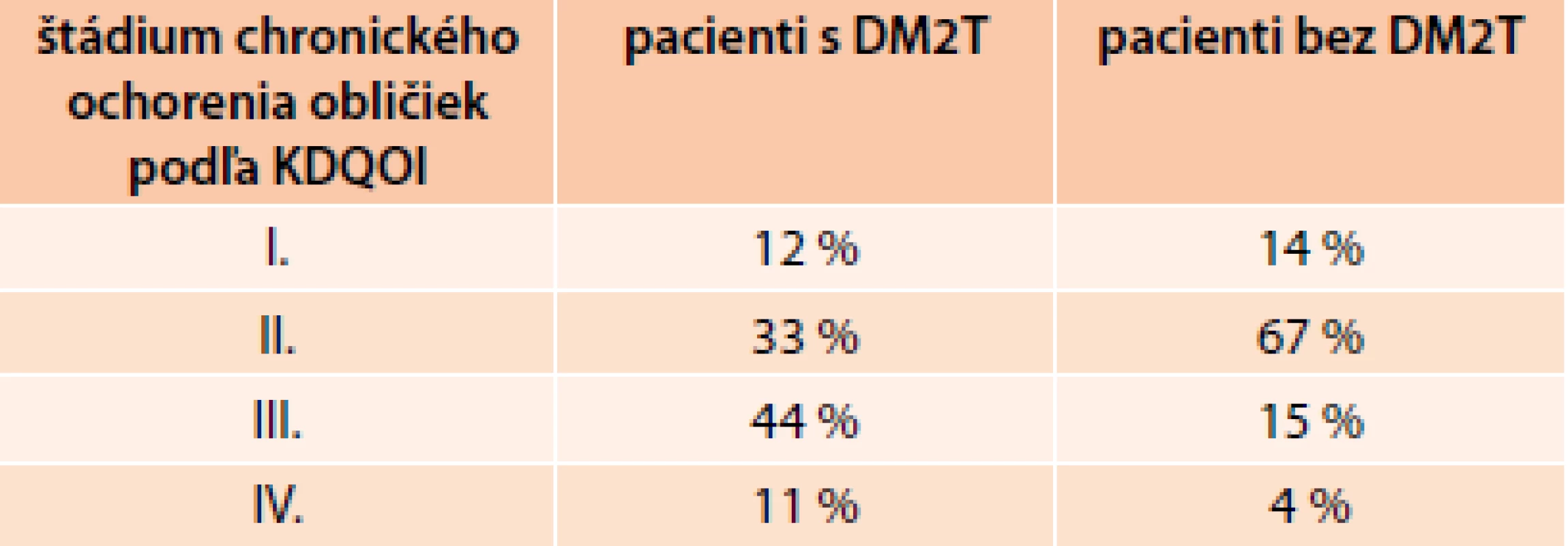
- klasifikáciu renálnej insuficiencie (podľa KDOQI) u týchto chorých uvádza tab. 3.
Prítomnosť chronickej renálnej insuficiencie mali všetci diabetici (priemerný vek 77 rokov) a 75 % nediabetikov (priemerný vek 80 rokov), pričom asi 60 % diabetikov a temer polovica nediabetikov trpela aj anémiou (hemoglobín < 130 g/l u mužov a < 120 g/l u žien). U diabetikov boli vyššie štádiá renálnej insuficiencie podľa klasifikácie KDOQI: III. štádium (44 % vs 15 % u nediabetikov) a IV. štádium (11 % vs 4 %).
Pacienti s diabetom boli ťažšie chorí ako nediabetici a ukazujú to tab. 1, 2 a 3, ktoré ukazujú, že hlavne frekvencia výskytu ale i intenzita kardiorenálneho syndrómu poukazujú, ako ťažko chorí s akútnym SZ sú u nás diabetici [2,3].

Čo na záver?
Výskyt renálnej insuficiencie/zlyhania je u osôb so SZ, hlavne chronickým, častý. A tak i výskyt kardiorenálneho syndrómu je častý, len ho takto treba v diagnózach aj písať, t. j. kategorizovať. Lepšou KV-liečbou a predlžovaním veku bude v budúcnosti iste stúpať. Poznanie patofyziológie syndrómu je dôležité, aby sme zlepšili prevenciu i liečbu tohto zložitého ochorenia.
prof. MUDr. Ján Murín, CSc.
jan.murin@gmail.com
I. interná klinika, LFUK a UN Bratislava
www.unb.sk
Doručené do redakcie 24. 8. 2015
Prijaté po recenzii 2. 10. 2015
Sources
1. Ronco C, House AA, Haapi M. Cardiorenal syndrome: refining the definition of a complex symbiosis gone wrong. Intensive Care Med 2008; 34(5): 957–962.
2. Pernický M, Murín J. Pacienti v ústavnej pohotovostnej službe na internej klinike. Vnit Lek 2010; 56(5): 47.
3. Pernický M, Murín J. Pacienti v pohotovostnej službe na internej klinike. Cardiology Lett 2010; 19(4): 287–292.
4. Pernický M, Karabová M, Murín J. Diabetes in acute heart failure and acute coronary syndrome – insight from a routine clinical practice in an Internal department with high volume of patients. Cardiology Lett 2012; 21(Suppl 1): S55
5. Pernický M, Karabová M, Murín J. Diabetes in acute heart failure and acute coronary syndrome. Eur J Heart Fail Supplements 2012; 14(Suppl A): S69.
6. Mc Alister FA, Ezekowitz J, Tonelli M et al. Renal insufficiency and heart failure: prognostic and therapeutic implications from a prospective cohort study. Circulation 2004; 109(8): 1004–1009.
7. Hillege HL, Girbes AR, de Kam PJ et al. Renal function, neurohormonal activation, and survival in patients with chronic heart failure. Circulation 2000; 102(2): 203–210.
8. Sarnak MJ. Cardiovascular complications in chronic kidney disease. Am J Kidney Dis 2003; 41 (Suppl 5): 11–17.
9. Henry RM, Kostense PJ, Bos G et al. Mild renal insufficiency is associated with increased cardiovascular mortality: The Hoorn Study. Kidney Int 2002; 62(4): 1402–1407.
10. Foley RN, Parfrey PS, Sarnak MJ. Epidemiology of cardiovascular disease in chronic renal disease. J Am Soc Nephrol 1998; 9(12 Suppl): S16-S23.
11. Fried LF, Shlipak MG, Crump C et al. Renal insufficiency as a predictor of cardiovascular outcomes and mortality in elderly individuals. J Am Coll Cardiol 2003; 41(8): 1364–1372.
12. Weinfeld MS, Chertow GM, Stevenson LW. Aggravated renal dysfunction during intensive therapy for advanced chronic heart failure. Am Heart J 1999; 138(2 Pt 1): 285–290.
13. Nohria A, Hasselblad V, Stebbins A et al. Cardiorenal interactions: insights frome the ESCAPE trial. J Am Coll Cardiol 2008; (3)51: 300–306.
14. Mullens W, Abrahams T, Skouri HN et al. Elevated intra-abdominal pressure in acute decomensated heart failure. J Am Coll Cardiol 2008; 51(3): 300–306.
15. Mullens W, Abrahams Z, Francis GS et al. Importance of venous congestion for worsening renal function in advaced decompensated heart failure. J Am Coll Cardiol 2009; 53(7):589–596.
16. Petersson M, Friberg P, Eisenhofer G et al. Long-term outcome in relation to renal sympathetic aktivity in patients with chronic heart failure. Eur Heart J 2005; 26(9): 906–913.
17. Remuzzi G, Perico N, Mancia M et al. The role of the renin-angiotensin-aldosteron system in the progression of chronic kidney disease. Kidney Int Suppl 2005; (99): S57-S65.
18. Tojo A, Onozato ML, Kobayashi N et al. Angiotensin II and oxidative stress in Dahl-sensitive rat with heart failure. Hypertension 2002; 40(6): 834–839.
19. Jie KE, Verhaar MC, Cramer MJ et al. Erythropoetin and the cardiorenal syndrome: cellular mechanisms on the cardiorenal conectors. Am J Physiol Renal Physiol 2006; 291(5): F932-F944.
20. Kostam MA, Gheorghiade M, Burnett JC Jr et al. Effects of oral tolvaptan in patients hospitalized for worsening heart failure: the EVEREST Outcome Trial. JAMA 2007; 297(12): 1319–1331.
21. Funaya H., Kitakaze M, Node K et al. Plasma adenosine levels increase in patients with chronic heart failure. Circulation 1997; 95(6): 1363–1365.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Forum Diabetologicum

2015 Issue 3
Most read in this issue
- Pohľad na kardiorenálny syndróm
- Najčastejšie infekčné komplikácie u diabetikov a ich liečba
- Výskyt diabetickej nefropatie v populácii pacientov s diabetes mellitus na Slovensku: výsledky prieskumu NEFRITI
- Včasný skríning a liečba spomaľujú progresiu diabetickej nefropatie
