Kyselina močová: patofyziologické implikácie
Uric acid: pathophysiological implications
Pathophysiologic relations of hyperuricaemia are complex and associations are cinfirmed with cardiovascular, renal, methabolic diseases, endothelial dys-function, arterial hypertension, systemic inflammation, proaggregation and oxidative stress. From the first scientific report about hyperuricaemia in 1871 repeatedly causal relationship of increased uric acid level to several organism´s systems is described.
Keywords:
acid uric – hyperuricemia – pathophysiology
Authors:
Fedor Šimko 1; Andrej Dukát 2
Authors‘ workplace:
Ústav patologickej fyziológie LF UK v Bratislave
1; V. interná klinika LF UK a UNB, Nemocnica Ružinov, Bratislava
2
Published in:
Forum Diab 2019; 8(1): 11-14
Category:
Review Article
Overview
Patofyziologické vzťahy hyperurikémie sú veľmi komplexné a asociácie sú dokázané s kardiovaskulárnymi ochoreniami, hypertenziou, systémovým zápalom, zníženou vazodilatačnou odpoveďou ciev, proagregačným stavom, endotelovou dysfunkciou a oxidačným stresom. Od prvej vedeckej správy o význame hyperurikémie v r. 1871 bol opakovane dokazovaný kauzálny vztah zvýšenej hladiny kyseliny močovej ku poruchám viacerých systémov organizmu.
Klíčová slova:
hyperurikémia – kyselina močová – patofyziológia
Úvod
Epidemiologické údaje o hyperurikémii sú jednoznačné. Tieto údaje uvádzajú výskyt hyperurikémie približne u 6 % mužov vo vekovej skupine ≥ 50 rokov v USA [1]. Za dvadsaťročie 1970–1990 ročná incidencia v USA stúpla z 20,2/100 000 na 45,9/100 000 ľudí [2]. Výskyt hyperurikémie v rôznych populáciách významne kolíše od 4 % až do 40 % v závislosti od rasových a geografických vplyvov. V nemocničnej populácii sa jej výskyt udáva okolo 7 % a slúži aj ako prediktor úmrtí počas hospitalizácie u pacientov (napr. so srdcovým zlyhávaním). V našich podmienkach výskyt dny v populácii predstavuje asi 1 % a hyperurikémie asi 5 %. V ambulanciách všeobecných lekárov pre dospelých pripadá v priemere na 1 500 pacientov asi 15 pacientov s dnou a 60 pacientov s hyperurikémiou.
Patofyziologické aspekty
Kyselina močová je chemicky 2,6,8-trihydroxypurín. U väčšiny cicavcov (okrem človeka) sa nachádza enzým urikáza, ktorý ju rozkladá. U človeka je kyselina močová konečným produktom metabolizmu purínových látok, okrem toho sa syntetizuje energeticky náročným spôsobom v pečeni. V obehovom systéme cirkuluje ako urát bez väzby na bielkoviny vo voľnej forme v tekutom stave krvi. Vo všetkých extracelulárnych tekutinách, v ktorých je hlavným katiónom sodík, je pH okolo 7,4–98 % kyseliny močovej vo forme monosódnej soli (monosodi-umurát). Pri prekročení indexu rozpustnosti kryštály, ktoré vznikajú v synoviálnej tekutine, alebo tofy u chorých s dnou, sú zložené z mononatriumurát monohydrátu. Uráty majú pritom vysokú antioxidačnú kapacitu. In vitro sledovania ukázali, že urát je účinný odpratávač (scavenger) reaktívnych kyslíkových radikálov. U zdravých osôb predstavujú uráty až 60 % celkovej antioxidačnej kapacity [3]. Referenčné populačné hodnoty kyseliny močovej v sére v priebehu života sú uvedené v tab. 1. V období pred pubertou je hladina kyseliny močovej nízka u oboch pohlaví. V puberte sa hladina urikémie prudko zvyšuje a neskôr sa u dievčat hladina zvyšuje iba mierne, a to až do menopauzy. U chlapcov sa v puberte zvyšuje veľmi prudko a zostáva potom v priebehu života na individuálne rovnakej úrovni. Hladina urikémie má teda pomerne široký populačný referenčný interval, ktorý sa za bežných okolností udržiava až do staroby, i keď aj tento podlieha aj malým chronobiologickým fluktuáciám [4]. Je teda výsledkom zvýšenej tvorby a zníženého vylučovania kyseliny močovej, alebo kombinácie oboch týchto uvedených príčin (tab. 2).
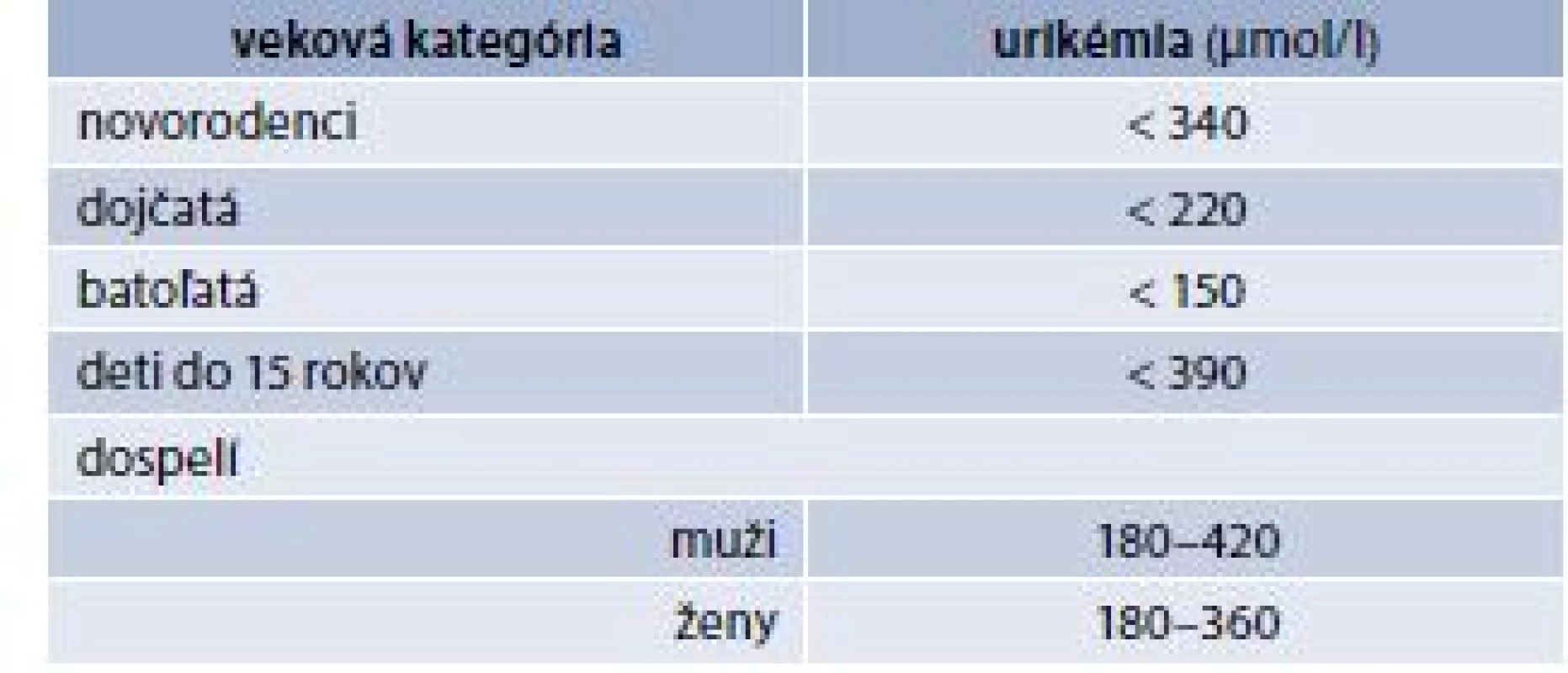
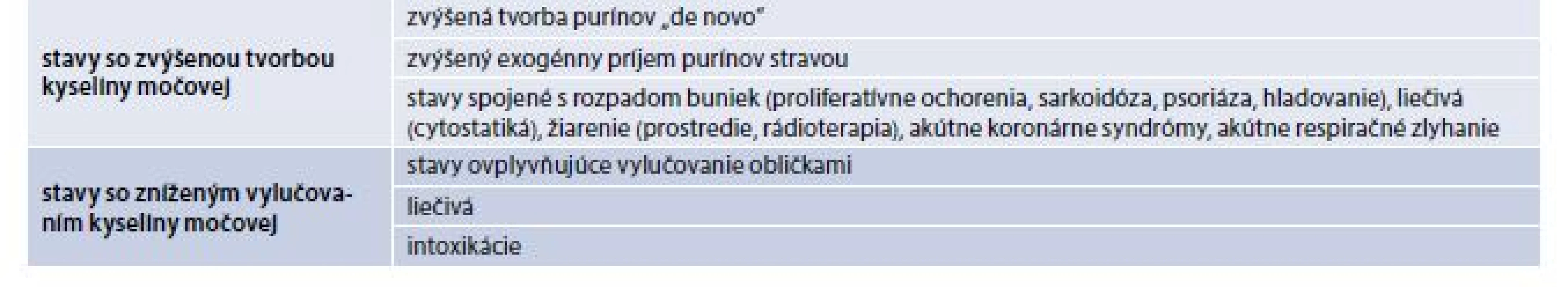
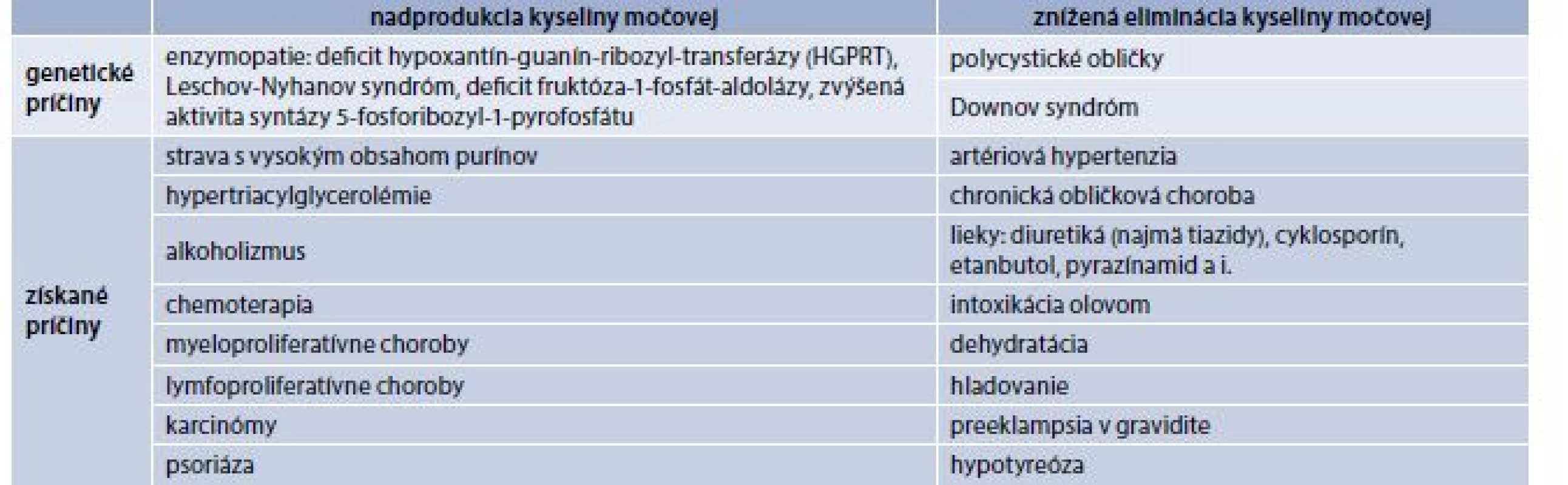
Endogénna tvorba kyseliny močovej je v značnej miere závislá od aktivity fosforibozyl-pyrofosfítu a deficitu hypoxantín-fosforibozyl-transferázy. Keďže až 70 % vylúčeného urátu sa uskutočňuje obličkami, hlavným určujúcim faktorom urikémie sú obličky. Zvyšok sa potom vylučuje gastrointestinálnym traktom: kyselinu močovú degradujú črevné baktérie na amoniak a oxid uhličitý. Prehľad homeostázy kyseliny močovej v organizme je schematicky znázornený na schéme. Tab. 3 potom uvádza najčastejšie vrodené a získané príčiny hyperurikémie. Tieto je možné v zásade rozdeliť do dvoch skupín: na situácie, v ktorých dochádza ku zvýšeniu tvorby kyseliny močovej, a na situácie, v ktorých dochádza ku zníženiu vylučovania kyseliny močovej. V tomto kontexte je napokon dôležité uviesť aj predpokladané teoretické vplyvy inhibície xantín-oxidázy:
- pokles endogénnej produkcie kyseliny močovej vedie ku zníženiu systémovej koncentrácie urátov
- pokles lokálnej spotreby molekulárneho kyslíka použitého na tvorbu xantínu a kyseliny močovej
- pokles tvorby lokálnych reaktívnych kyslíkových radikálov a zníženie oxidatívneho stresu
- pokles v katabolizme adenozín-monofosfátu vedie ku zlepšeniu energetiky v tkanivách
- pokles v katabolizme vazodilatačného kysličníka dusnatého
#543532
Klinické implikácie
Kyselina močová je jedným (i keď nie jediným) mechanizmom vedúcim ku progresii obličkového ochorenia. Vedie ku transformácii renálnych tubulárnych buniek na fibroblasty (transformácia epiteliálnych buniek na mezenchymálne v interstíciu je novým a doposiaľ neznámym mechanizmom). Aj samotná infúzia kyseliny močovej v experimente vedie ku zápalovej reakcii v obličke a zápal je spúšťacím mechanizmom (triggerom) progresie obličkového ochorenia. Liečbou na každé zníženie kyseliny močovej o 1 mg/dl dochádza ku zlepšeniu glomerulárnej filtrácie o 1,15 ml/min v porovnaní s neliečenými. Kyselina močová (diétne faktory, inzulínová rezistencia, liečba diuretikami) je amplifikátorom progresie straty renálnych funkcií a naopak jej zníženie liečbou alopurinolom vedie ku spomaleniu rýchlosti poklesu renálnych funkcií [5]. Z realizovaných 11 prospektívnych štúdií vo vzťahu zvýšenej kyseliny močovej k poklesu glomerulovej filtrácie a incidencii chronickej obličkovej choroby sa ukázalo na každé zvýšenie jej hladiny o 1 mg/dl relatívne riziko RR: 1,18 (95% CI 1,15–1,22) [6]. Kyselina močová je vôbec nezávislým rizikovým faktorom pre progresiu zníženia renálnej funkcie počas 5-ročného sledovania u zdravých osôb (darcov krvi) [7]. Už dávnejšie sa ukázal vzťah medzi hyperurikémiou a hypertenziou. Pri akútnom zvýšení kyseliny močovej v sére dochádza k okamžitému zvýšeniu hodnôt krvného tlaku [8]. Chronické zvýšenie vedie ku pretrvávaniu abnormálnych hodnôt krvného tlaku a vyvoláva aj ireverzibilné cievne zmeny aj zmeny v glomeruloch, ktoré napokon vedú k fixovaniu hypertenzie citlivej na soľ [9]. Včasné objavenie sa hyperurikémie je spoľahlivým prediktorom neskoršieho rozvoja hypertenzie. Národný prieskum NHANES v USA ukázal, že hyperurikémia je nezávislým prediktorom kardiovaskulárnej mortality osôb nad 45 rokov, bez ohľadu na pohlavie, menopauzálny stav, liečbu diuretikami, prítomnosti kardiovaskulárneho ochorenia, alebo na rasové rozdiely [10].
Z realizovaných 8 prospektívnych štúdií vo vzťahu zvýšenej kyseliny močovej ku diabetes mellitus sa ukázalo na každé zvýšenie jej hladiny o 1 mg/dl relatívne riziko (RR: 1,06 (95% CI 1,04–1,07). Z veľkej medzinárodnej INTERHEART štúdie (realizovanej na všetkých kontinentoch sveta a v rôznych populáciách) vieme, že hladina kyseliny močovej koreluje s telesnou hmotnosťou, hyperurikémia je prítomná až u 80 % pacientov s metabolickým syndrómom a diabetes mellitus, je prítomná u 70 % pacientov s komorbiditami: hypertenziou a diabetes mellitus [11,12]. Vzťah hyperurikémie ku kardiovaskulárnym ochoreniam je teda dokázaný dostatočne a jednoznačne [13]. Hyperurikémia je spojená s endotelovou dysfunkciou a normalizácia jej hodnôt liečbou a kontrola a eliminácia ďalších rizikových faktorov jasne zlepšujú endotelovú funkciu [14,15].
Napokon je dôležité ešte uviesť škálu diferenciálnej diagnostiky. Diferenciálna diagnostika hyperurikémie, choroby a poruchy je veľmi rozsiahla. Obsahuje nasledovné:
- vaskulárne: dysfunkcia endotelu, ateroskleróza a všetky jej klasické rizikové faktory, metabolický syndróm, arterioloskleróza, diabetická makro- a mikroangiopatia, Mönckebergova medioskleróza (mediokalcinóza), vaskulitídy, chronická vénová choroba dolných končatín, flebotrombóza a tromboembolická choroba
- onkologické: zhubné nádory, malígne procesy a ich liečba
- choroby srdca: ischemická choroba srdca (všetky formy, vrátane akútnych koronárnych syndrómov, srdcové zlyhávanie)
- choroby mozgu: náhle mozgové cievne príhody a iné formy ischemickej choroby mozgu
- choroby obličiek: akútne a chronické glomerulonefritídy, tubulointersticiálne nefritídy vrátane dnavej nefropatie, urátová nefrolitiáza
- choroby pľúc: akútne respiračné infekcie, chronická respiračná insuficiencia
- choroby krvi: (trombofilné stavy, lymfoproliferatívne a myeloproliferatívne stavy, niektoré anémie
- endokrínne choroby: diabetes mellitus, hypotyreóza, hyperparatyreóza a hypoparatyreóza, diabetes insipidus
- choroby pohybového systému: arthritis urica, alkaptonúria, reumatoidná artritída, systémový lupus erythematosus
- choroby pečene: steatóza a cirhóza pečene, dyslipoproteinémie, lipidózy, glykogenózy, amyloidóza
- infekčné choroby: tuberkulóza, infekčná mononukleóza
- intoxikácie: mykointoxikácie (1. a 8. typ), otrava olovom, otrava metylalkoholom
- genetické poruchy: Downov syndróm, Leschov-Nyhanov syndróm
- iné: preeklampsia a eklampsia, dehydratácia, psoriáza, lieky: diuretiká, salicyláty, kyselina nikotínová, antituberkulotiká, cyklosporín
Záver
Patofyziologické vzťahy hyperurikémie sú veľmi komplexné a asociácie sú dokázané s kardiovaskulárnymi ochoreniami, hypertenziou, systémovým zápalom, zníženou vazodilatačnou odpoveďou ciev, proagregačným stavom, endotelovou dysfunkciou a oxidačným stresom.
prof. MUDr. Fedor Šimko, CSc., FESC
Doručené do redakcie 17. 12. 2018
Prijaté po recenzii 20. 2. 2019
Sources
- Zhu Y, Pandya BJ, Choi HK. Prevalence of gout and hyperuricemia in the US general population: the National Health and Nutrition Examination Survey 2007–2008. Arthritis Rheum 2011; 63(10): 3136–3141. Dostupné z DOI: <http://dx.doi.org/10.1002/art.30520>.
- Whelton A. Hyperuricemia and hypertension. A Confluence of Concepts. Editorial Commentary. Hypertension 2012; 60(5): 1112–1113. Dostupné z DOI: <http://dx.doi.org/10.1161/HYPERTENSIONAHA.112.198341>.
- Gavorník P, Dukát A, Gašpar L et al. Klinický význam a liečba hyperurikémie. Slov Klin Pr 2007; 1(1): 18–20.
- Najmik P. Hyperurikémia. Súč Klin Prax 2007; 4(1): 14–18.
- Masuo K, Kawaguchi H, Mikami H at al. Serum uric acid and plasma norepinephrine concentrations predict subsequent weight gain and blood pressure elevation. Hypertension 2003; 42(4): 474–480. Dostupné z DOI: <http://dx.doi.org/10.1161/01.HYP.0000091371.53502.D3>.
- Lai S, Mariotti A, Coppola B et al. Uricemia and homocysteinemia: nontraditional risk factors in the early stages of chronic kidney disease. Eur Rev Med Pharmacol Sci 2014; 18(7): 1010–1017.
- Johnson RJ, Kang DH, Feig D et al. Is there a pathogenic role of uric acid in hypertension and cardiovascular and renal disease? Hypertension 2003; 41(4): 1183–1190. Dostupné z DOI: <http://dx.doi.org/10.1161/01.HYP.0000069700.62727.C5>.
- Tangri N, Weiner DE. Uric acid, CKD, and cardiovascular disease: confounders, culprits and circles. Am J Kidney Dis 2010; 56(2): 247–250. Dostupné z DOI: <http://dx.doi.org/10.1053/j.ajkd.2010.06.004>.
- Špinar J, Vítovec J, Pařenica J. Hypertenze a hyperurikemie. Vnitř Lék 2005; 51(1): 82–86.
- Kang DH, Nakagawa T, Feng L et al. A role for uric acid in the progression of renal disease. J Am Soc Nephrol 2002; 13(12): 2888–2897.
- Loeffler LF, Navas-Acien A, Brady TM et al. Uric acid level and elevated blood pressure in US adolescents: National Health and Nutrition Examination Survey, 1999–2006. Hypertension 2012; 59(4): 811–817. Dostupné z DOI: <http://dx.doi.org/10.1161/HYPERTENSIONAHA.111.183244>.
- Šimko F, Šimko J, Fábryová M. ACE-Inhibition and Angiotensin II Receptor Blockers in Chronic Heart Failure: Patophysiological Consideration of the Unresolved Battle. Cardiovasc Drugs Ther 2003; 17(3):287–280.
- Khosla UM, Zharikov S, Finch JL et al. Hyperuricemia induces endothe-lial dysfunction. Kidney Int 2005; 67(5): 1739–1742. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1523–1755.2005.00273.x>.
- Price KL, Sautin YY, Long DA et al. Human vascular smooth muscle cells express a urate transporter. J Am Soc Nephrol 2006; 17(7): 1791–1795. Dostupné z DOI: <http://dx.doi.org/10.1681/ASN.2006030264>.
- Keenan S. Relation of Uric Acid to Serum Levels of High-Sensitivity CRP, Triglycerides, and HDL-C and to Hepatic Steatosis. Am J Cardiol 2012; 110(12): 1787–1792. Dostupné z DOI: <http://dx.doi.org/10.1016/j.amjcard.2012.08.012>.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Forum Diabetologicum

2019 Issue 1
Most read in this issue
- Dna ako staronový problém ambulantného lekára
- Liečba hyperurikémie
- Hyperurikémia a kardiovaskulárne ochorenia
- Kyselina močová: patofyziologické implikácie
