Riziko liečby inhibítormi protónovej pumpy vo vzťahu ku ochoreniu SARS-CoV-2
Authors:
Peter Vaňuga 1; Juraj Payer 2; Milan Kriška 3; František Sándor 4; Andrej Dukát 2
Authors‘ workplace:
Národný endokrinologický a diabetologický ústav, n. o., Ľubochňa
1; V. interná klinika LF UK a UNB, Nemocnica Ružinov, Bratislava
2; Ústav farmakológie a klinickej farmakológie LF UK v Bratislave
3; Klinika pneumológie a ftizeológie LF UK a UNB, Nemocnica Ružinov, Bratislava
4
Published in:
Forum Diab 2022; 11(1): 39-42
Category:
Overview
Medicína v dobe pandémie SARS-CoV-2 našu klinickú prax postavila pred celkom nové problémy. Jedným z nich predstavujú aj riziká pre toto infekčné ochoreníe. Okrem všeobecne známych rizík, ako je vek a komorbidity, sa ukázala byť dôležitá aj trvajúca zavedená liečba pacientov. V tomto kontexte je potrebné sa zamerať na jednu skupinu liekov vo farmakoterapii – PPI, nakoľko sa jedná o veľmi častú liečbu v klinickej praxi všade vo svete. Diskusie o tejto liečbe sa s poznatkami vyvíjajú a stále pokračujú.
Klíčová slova:
liečba – PPI – SARS-CoV-2
Úvod
Prvá práca, ktorá upozornila na možný vzťah liečby inhibítormi protónovej pumpy (Proton Pump Inhibitors – PPI) s infekciou COVID-19 bolo sledovanie v rámci národného gastroenterologického programu v USA, ktorý bol realizovaný medzi 3. májom a 24. júnom 2020 [1]. Išlo o dotazníkový prieskum, v ktorom zúčastnené osoby odpovedali na otázky o gastroenterologických symptómoch, súčasnom užívaní PPI a výsledkom testov na COVID-19. Otázky smerovali aj ku liečbe agonistami H2-receptorov – H2RA (známe ako H2-blokátory), ktoré sa používajú v liečbe v rovnakej indikácii, avšak natoľko neznižujú aciditu žalúdka, ako je to pri liečbe PPI. Bolo kontaktovaných 264 058 pacientov, z nich bolo následne sledovaných a vyhodnotených 86 602. Z tohto súboru 53 130 pacientov popisovalo prítomnosť abdominálneho diskomfortu, reflux žalúdka, pálenie a regurgitáciu. Táto skupina bola cielene dotazovaná na liečbu PPI a H2RA. Pozitívny test na SARS-CoV-2 malo 6,4 %. Adjustácia bola na vek, pohlavie, etnicitu, vzdelanie, prítomnosť dráždivého hrubého čreva, céliakie, refluxovej choroby, cirhózu pečene, Crohnovu chorobu, ulceratívnu kolitídu, diabetes mellitus a HIV/AIDS. Analýza údajov ukázala, že tí pacienti, ktorí užívali PPI 1-krát denne, mali 2-násobnú pravdepodobnosť pozitivity COVID-19 testu než tí, ktorí PPI neužívali: OR 2,15 (95% CI 1,90–2,44). Tí pacienti, ktorí užívali PPI 2-krát denne, mali až 4-násobnú pravdepodobnosť pozitivity testu: OR 3,67 (95% CI 2,93–4,60). Na druhej strane, liečba H2-blokátormi 1-krát denne mala o 15 % nižšiu pravdepodobnosť pozitivity COVID-19 testu: OR 0,85 (95 % CI 0,74–0,99). Celkové riziko je teda 3,7-násobné, bez potreby vynechať liečbu PPI, ak je táto indikovaná, avšak v dávkovaní raz denne. V súčasnosti sa tento súbor pacientov analyzuje na testovanú hypotézu, že H2RA môžu predstavovať ochranu pred týmto ochorením nezávisle od pH žalúdka.
Dotazníkové sledovanie poukázalo teda na asociáciu medzi liečbou PPI a pozitivitou COVID-19 testu. Podporilo však tézu, že gastrointestinálny trakt sa môže zúčastňovať na prenose SARS-CoV-2. Menej významný sa ukazuje prenos vírusu potravinami, teda fekálne-orálnou cestou, ale viac fekálne-respiračnou cestou (napr. aj splachovanie v toalete cez exhaláciu). Tento survey prekvapil aj výsledkom 6,4% pozitivity testov respondentov, keďže sa popisovala diagnostika u menej ako 1 % v celkovej americkej populácii. Aj keď nie je možné uvedené výsledky extrapolovať na celú americkú populáciu, predsa len je zrejmé, že respondenti popisovali nielen respiračné, ale aj gastrointestinálne príznaky: infekcia COVID-19 ich totiž tiež spôsobuje.
Inhibítory protónovej pumpy sa v súčasnosti dostali medzi 10 najpoužívanejších liekov vo svete, často sú predpisované bez jasnej indikácie (až v 70 % prípadov) [2]. Liečba PPI je rizikovým faktorom pre rotavírusy, chrípku, alebo norovírusy, ale aj pre gastroenteritídu počas obdobia najvyššej cirkulácie enterovírusov. Jednou z hlavných funkcií žalúdočnej šťavy je totiž inaktivovať prehltnuté mikroorganizmy, a tým inhibovať infekčné agens, ktoré dosiahnu črevo. Znížením žalúdočnej acidity pri liečbe PPI sa zvyšuje náchylnosť na vírusové chrípkové infekcie [3]. Riziko norovírusovej infekcie je OR 1,73 (95% CI 1,07–2,81; p = 0,02) [22]. COVID-19 býva vo svojom priebehu často komplikovaný sekundárnymi infekciami liečbou PPI a rizikom akútnej gastroenteritídy: RR 1,81 (95% CI 1,72–1,90) [4]. Vírus SARS-CoV-2 využíva receptor ACE2 na vstup do enterocytov. Liečbou PPI sa zvyšuje pH v žalúdku nad 3, čo umožňuje vírusu ľahší vstup cez GIT, vedie ku enteritíde, kolitíde a jeho systémovému rozšíreniu do ďalších orgánov, vrátane postihnutia pľúc.
Vo vzťahu ku SARS-CoV-2 infekcie sa ukázalo, že dochádza ku infekcii gastrointestinálnych glandulárnych epitelových buniek [5]. Infikovaní pacienti s prítomnou gastrointestinálnou symptomatológiou pritom majú závažnejšiu pneumóniu [6]. Infekcia býva často komplikovaná sekundárnymi infekciami a rozvojom akútneho respiračného distres syndrómu s vysokou morbiditou a mortalitou [7].
V tomto kontexte bola realizovaná nemecká retrospektívna štúdia zameraná na sledovanie vplyvu liečby PPI na priebeh hospitalizácie u takto infikovaných pacientov [8]. U tretiny hospitalizovaných pacientov (31,6 %) bol priebeh komplikovaný sekundárnymi infekciami. U pacientov liečených PPI to predstavovalo 48,4 % v porovnaní s výskytom sekundárnych infekcií neliečených PPI – 20,0 % (p < 0,001). PPI predstavovali významný prediktívny rizikový faktor pre rozvoj sekundárnej infekcie: OR 2,37 (95% CI 1,08–5,22; p = 0,032). Potvrdili sa tak výsledky už starších metaanalýz [9]. Aj prítomnosť gastroezofageálnej refluxovej choroby je významným nezávislým prediktívnym rizikovým faktorom sekundárnej infekcie: OR 6,4 (95% CI 1,50–35,51; p = 0,034), čo svedčí o význame mikroaspirácie v patogenéze sekundárnej infekcie v tejto skupine pacientov. Liečba PPI má nepriamy vplyv na rozvoj syndrómu dychovej tiesne (ARDS – Adult Respiratory Distress Syndrome) spúšťačom sekundárnej infekcie. ARDS sa vyskytol v 48,4 % prípadov pacientov liečených PPI v porovnaní s 12,3 % bez liečby (p = 0,020). Takto liečení pacienti mali aj významne vyšší index mortality (19,4 % vs 5,6 %; p = 0,010. Aj v kontexte tejto štúdie je liečba PPI spojená s vyšším rizikom sekundárnych infekcií a ARDS, a preto by mala byť zavedená s veľkou opatrnosťou a iba na kratšiu dobu [10].
Mikrobiálna sprevádzajúca infekcia pri COVID-19
Mikrobiálna sprevádzajúca infekcia hrá veľmi dôležitú úlohu v rozvoji infekcie SARS-CoV-2 [11]. Podieľa sa na celom procese rozvoja, priebehu aj prognózy ochorenia. Na tejto koinfekcii sa podieľa viacero patogénov: vírusy, baktérie a huby, čo predstavuje ďalšie problémy v diagnostike, liečbe a prognóze COVID-19. Podieľa sa na vyššej symptomatológii ochorenia i následnej mortalite infikovaných pacientov.
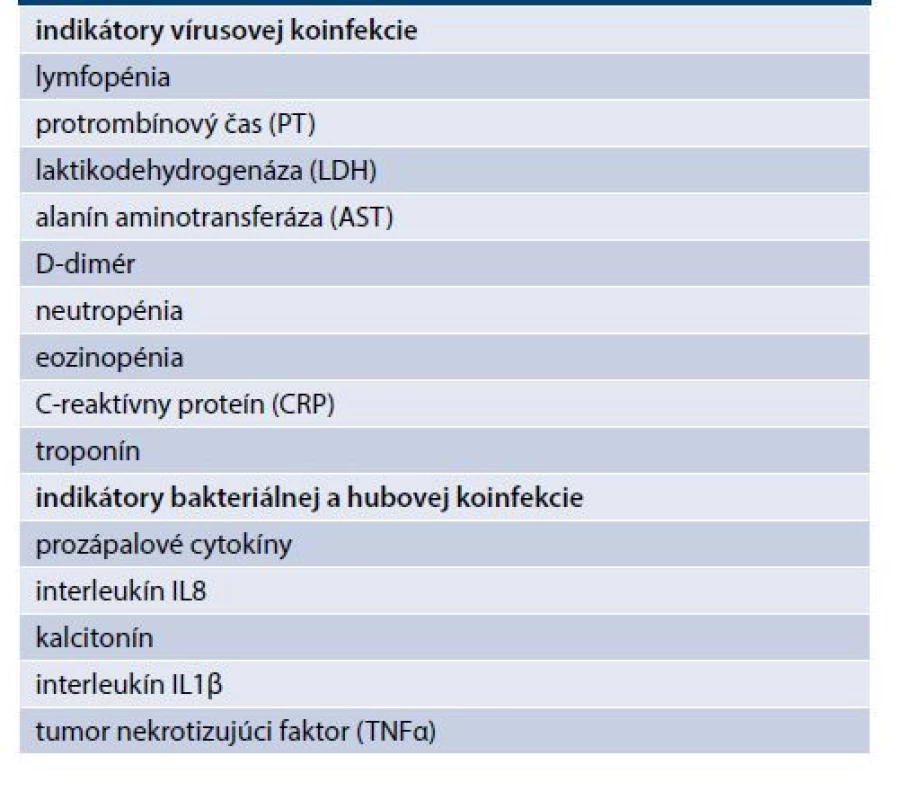
Koinfekcia vírusmi pri respiračných ochoreniach je veľmi častá a má aj svoje regionálne rozdiely. Predstavujú ju najmä enterovírusy a rinovírusy, humánny metapneumovírus, respiračný syncytiálny vírus, ďalšie koronavírusy (nonCOVID-19), vírus parainfluenzy 2 a 3. Často popisované sú aj infekcie Chlamydia pneumoniae, influenzy A a Mycoplasma pneumoniae [11]. Bakteriálna a hubová koinfekcia majú významný vplyv na progresiu a prognózu ochorenia, zvlášť u ťažkých pacientov. V týchto prípadoch môže vyžadovať intenzívnu starostlivosť, potrebu antibiotickej liečby a má významne vyššie riziko mortality [12]. Koinfekcia zvyšuje stupeň systémového zápalu, a tým sa spolupodieľa na závažnosti ochorenia a predlžuje proces hojenia. Bakteriálna a hubová koinfekcia je spojená s 2,5-násobne zvýšeným rizikom úmrtia na SARS-CoV-2 [13]. Aj tu sa potvrdzuje významná úloha črevného mikrobiómu [14]. Indikátory nápomocné v diagnostike sú uvedené v prehľade v tab. 1 a tab. 2.

Liečba PPI a prognostické riziko pri COVID-19
Význam uvedených skutočností podčiarkuje ale fakt, že PPI a gastroprotekcia patria ku štandardnej podpornej liečbe závažne chorých pacientov a tých, ktorí sú intubovaní [15]. Liečba u pacientov s pneumóniou ale má vedľajšie nežiaduce účinky spojené s asistovanou ventiláciou, a dokonca i s mortalitou [16].
Iba celkom nedávno boli publikované výsledky veľkej národnej epidemiologickej štúdie z Južnej Kórei zo vzorky 132 316 pacientov vo veku viac ako 18 rokov, ktorí boli testovaní na SARS-CoV-2, z ktorej bolo na liečbe PPI 14 163.
U pacientov, u ktorých bolo potvrdené ochorenie, súčasné užívanie PPI predstavovalo významné riziko závažného priebehu (79 %), kým vzťah ku minulému užívaniu PPI ostal nesignifikantný. Súčasné užívanie PPI (počas posledných 30 dní) bol spojený s 90% zvýšeným rizikom závažných komplikácií. Táto medikácia nezvyšovala riziko SARS-CoV-2 infekcie v kórejskej populácii. Akokoľvek však i krátkodobá liečba PPI významne zvyšovala riziko horšieho priebehu ochorenia.
Metaanalýza na 195 230 pacientoch ukázala, že súčasná liečba PPI zvyšuje riziko mortality na COVID-19: OR 1,67 (95% CI 1,41–1,97) [17]. Je však potrebné pripomenúť existujúcu heterogenitu pri analyzovaných štúdiách a ich značné regionálne rozdiely (napr. medzi Čínou a USA) a rozdielne dávkovacie režimy a trvanie liečby [18].
Iba pred mesiacom bola publikovaná v tomto kontexte posledná a veľmi dôležitá informácia, ktorá sa týka liečby PPI. Upozornila na fakt, že pravidelná liečba touto skupinou liekov je spojená s vyšším rizikom aj mozgovocievnej príhody. Ukázala to prospektívna kohortová štúdia 492 479 probandov vo veku 37–73 rokov z Biobanky vo Veľkej Británii (roky 2006–2010) a metaanalýza 9 randomizovaných kontrolovaných štúdií 26 642 pacientov [19]. Pravidelné užívanie PPI pri prospektívnom sledovaní bolo spojené s vyšším rizikom mozgovocievnej príhody: HR 1,16 (95% CI 1,06–1,27). Metaanalýza preukázala, že toto riziko predstavuje RR 1,22 (95% CI 1,00–1,50) [19]. Bolo prepočítané bazálne Framinghamské rizikové skóre mozgovocievnej príhody počas obdobia 5 rokov na jednotlivé kvartily. Rozdiely rizika v kvartiloch predstavujú 1,34 %, 3,32 %, 4,83 % a 6,28 %. Čisté riziko teda závisí od východzieho základného globálneho rizika daného pacienta. V klinickej praxi je teda potrebné pri pravidelnej preskripcii vychádzať zo skórovacieho systému jednotlivého pacienta.
Záver
Metaanalýzy randomizovaných kontrolovaných štúdií ukázali, že liečba PPI zvyšuje riziko črevných infekcií, ktoré sú v súvislosti s liečbou navodenej hypochlórhydrii [20]. Napriek tomu, že vplyv potlačenia acidity pri infekcii SARS-CoV-2 nie je celkom známy, pH < 3 zhoršuje infekčnosť podobnej infekcie SARS-CoV-1. Keďže SARSCoV- 2 je dokázaný enteropatický vírus, vážne sa uvažuje o možnosti, že PPI zvyšujú riziko infekcie týmto vírusom [21].
Najvyššie riziko predstavuje liečba PPI v dávke 2-krát denne. Liečba H2-blokátormi v tomto kontexte nepredstavuje také riziko, ako liečba PPI. Kým nebudeme mať dostatok definitívnych dôkazov, pre klinickú prax sa doporučuje liečbu PPI v najnižších dávkach a 1-krát denne po čo najkratšiu dobu [22].
Z tohto hľadiska je potrebné, aby klinici uvažovali o zistenom riziku pri tejto liečbe svojich pacientov, zvažovali riziko a benefit v manažmente svojich pacientov v rámci personalizovanej medicíny a v čase pandémie prehodnotili reálnu potrebu PPI u pacientov, ktorí ju nepotrebujú [23].
Doručené do redakcie | Received 3. 1. 2022
Prijaté po recenzii | Accepted 14. 2. 2022
prof. MUDr. Andrej Dukát, CSc., FRCP
www. fmed.uniba.sk
Sources
1. Almano CHV, Chey WD, Spiegel MBR. Increased Risk of COVID-19 Among Users of Proton Pump Inhibitors. Am J Gastroenterol 2020; 115(10): 1707–1715. Dostupné z DOI: <http://dx.doi.org/10.14309/ajg.0000000000000798>
.2. Marks D. Time to halt the overprescribing of proton pump inhibitors. Clin Pharm 2016; 8(8). Dostupné z DOI: <http://dx.doi.org/doi.org/10.1211/CP.2016.20201548>.
3. Martinsen TC, Fossmark R, Waldum HL. The phylogeny and biological function of gastric juice-microbiological cosequences of removing gastric acid. Int J Mol Sci 2019; 20(23): 6031. Dostupné z DOI: <http://dx.doi.org/doi.org/10.3390/ijms.20236031>.
4. Vilcu AM, Sabatte L, Blanchon T et al. Association between acute gastroenteritis and continuous use of proton pump inhibitors during winter periods of highest circulation of enteric viruses. JAMA Netw Open 2019; 2(11): e1916205. <http://dx.doi.org/10.1001/jamanetworkopen.2019.16205>.
5. Xiao F, Tamg M, Zheng X ei al. Evidence for gastrointestinal infection of SARS-CoV-2. Gastroenterology 2020: 158(6): 1831–1833. Dostupné z DOI: <http://dx.doi.org/10.1053/j.gastro.2020.02.055>.
6. Zhang H, Liao YS, Gong J et al. Clinical characteristics of coronavirus disease (COVID-19) patients with gastrointestinal symptoms: a report of 164 cases. Dig Liver Dis 2020; 52(10): 1076–1079. Dostupné z DOI: <http://dx.doi.org/doi.org/10.1016/j.dld.2020.04.034>.
7. Huang C, Wang Y, Li X et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet 2020; 395(10223): 497–506. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(20)30183–5>.
8. Luxenburger H, Sturm L, Biever P et al. Treatment with proton pump inhibitors increases the risk of secondary infections and ARDS in hospitalized patients with COVID-19: coincidence or underestimated risk factor? J Intern Med 2021; 289(1): 121–124. Dostupné z DOI: <http://dx.doi.org/10.1111/joim.13121>.
9. Eom CS, Jeon CY, Lim JW et al. Use of acid-suppressive drugs and risk of pneumonia: a systematic review and meta-analysis. CMAJ 2011; 183(3): 310–319. Dostupné z DOI: <http://dx.doi.org/10.1503/cmaj.092129>.
10. Charpiat B, Bleyzac N, Tod M. Proton Pump Inhibitors are Risk Factors for Viral Infections: Even for COVID-19? Clin Drug Invest 2020; 40(10): 897–899. Dostupné z DOI: <http://dx.doi.org/10.1007/s40261–020–00963-x>.
11. Chen X, Liao B, Cheng L et al. The microbial coinfection in COVID-19. Appl Microbiol Biotechnol 2020; 104/18): 7777–7785. Dostupné z DOI: <http://dx.doi.org/10.1007/s00253–020–10814–6>.
12. Lim YK, Kweon OJ, Kim HR et al. Impact of bacterial and viral coinfection in community-acquired pneumonia in adults. Diagn Microbiol Infect Dis 2019; 94(1): 1: 50–54. Dostupné z DOI: <http://dx.doi.org/10.1016/j.diagmicrobio.2018.11.014>.
13. Martins-Filho PR, Tavares CSS, Santos VS. Factors associated with mortality in patients with COVID-19. Eur J Intern Med 2020; 76: 97–99. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ejim.2020.04.043>.
14. Dukát A, Kubíková E, Payer J, Šimko F. Aké sú možné úlohy črevného mikrobiómu v procese vývoja endotelovej dysfunkcie a následnej aterosklerózy? Int Med 2018; 18(9): 383–385.
15. Homolak J, Kodvanj I, Trkulja V. An Additional Perspective on Proton Pump Inhibitors as Risk Factors for COVID-19. Clin Drug Invest 2021; 41(3): 287–289. Dostupné z DOI: <http://dx.doi.org/10.1007/s40261–021–01007–8>.
16. Lee SW, Ha EK, Yeniova AO et al. Severe clinical outcomes of COVID-19 associated with proton pump inhibitors: a nationwide cohort study with propensity score matching. Gut 2021; 70(1): 76–84. Dostupné z DOI: <http://dx.doi.org/10.1136/gutjnl-2020.322248>.
17. Toubasi AA, AbuAzenh RB, Khraisat BR et al. Proton Pump Inhibitors: Current Use and the Risk of Coronavirus Infectious Disease 2019 Development and its Related Mortality. Meta-analysis. Arch Med Res 2021; 52(6): 656–659. Dostupné z DOI: <http://dx.doi.org/10.1016/j.arcmed.2021.03.004>.
18. Li GF, An XX, Yu Y et al. Do proton pump inhibitors influence SARS-CoV-2 related outcomes? A meta-analysis. BMJ Gut 2021; 70(9): 1806–1808. Dostupné z DOI: <http://dx.doi.org/10.1136/gutjnl-2020–323366>.
19. Yang M, He Q, Gao F et al. Regular use of proton-pump inhibitors and risk of stroke: a population-based cohort study and meta-analysis of randomized-controlled trials. BMC Medicine 2021: 19(1): 316. Dostupné z DOI: <http://doi.org/10.1186/s12916–021–02189–5>.
20. Lim YK, Kweon OJ, Kim HR et al. Impact of bacterial and viral coinfection in community-acquired pneumonia in adults. Diagn Microbiol Infect Dis 2019; 94(1):50–54. Dostupné z DOI: <http://dx.doi.org/10.1016/j.diagmicrobio.2018.11.014>.
21. Xiao F, Tamg M, Zheng X et al. Evidence for gastrointestinal infection of SARS-CoV-2. Gastroenterology 2020; 158(6): 1831–1833. Dostupné z DOI: <http://dx.doi.org/10.1053/j.gastro.2020.02.055>.
22. Prag C, Prag M, Fredlund H. Proton pump inhibitors as a risk factor for norovirus infection. Epidemiol Infect 2017; 145(8): 1617–1623. Dostupné z DOI: <http://dx.doi.org/10.1017/S0950268817000528>.
23. Kow CHB, Hasan SS. Use of proton pump inhibitors and risk of adverse clinical outcomes from COVID-19: a meta-analysis. J Int Med 2021; 289(1): 125–128. Dostupné z DOI: <http://dx.doi.org/10.1111/joim.13183>.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Forum Diabetologicum

2022 Issue 1
Most read in this issue
- Persisting long-COVID-19 syndrome
- Diabetes mellitus and COVID-19: reciprocal relationship
- Diabetes and obesity (diabesity) and COVID-19
- Risk of proton pump inhibitors treatment in relationship to SARS-CoV-2 disease
