Manažment hypertriacylglycerolémie z pohľadu najnovších odporúčaní Americkej endokrinologickej spoločnosti (The Endocrine Society)
Management of hypertriacylglycerolaemia from the point view of newest guidelines of The Endocrine Society
One of the major modifiable risk factor of atherosclerosis is atherogenic dyslipidemia characterized by hypertriglyceridemia, low levels of HDL-cholesterol and the presence of small dense LDL particles. Various recommendations are dedicated to management of disorders of lipid metabolism. In September 2012 The Endocrine Society released its recommendations to the management of hypertriglyceridemia.
Key words:
atherosclerosis – atherogenic dyslipidemia – dyslipoproteinemia – hypertriglyceridemia
Autoři:
Peter Jackuliak; Miriam Avramovová; Juraj Payer
Působiště autorů:
V. interná klinika Lekárskej fakulty UK a UNB, Nemocnica Ružinov, Bratislava, prednosta prof. MUDr. Juraj Payer, CSc.
Vyšlo v časopise:
Forum Diab 2013; 2(2): 140-145
Kategorie:
Diabetológia aktuálne
Souhrn
Jedným z hlavných ovplyvniteľných rizikových faktorov aterosklerózy je aterogénna dyslipidémia charakterizovaná hypertriacylglycerolémiou, nízkymi hodnotami HDL-cholesterolu a prítomnosťou malých denzných LDL-častíc. Práve manažmentu porúch lipidového metabolizmu sa venujú rôzne odporučenia. V septembri 2012 aj Americká endokrinologická spoločnosť vydala svoje odporučenia k manažmentu hypertriacylglycerolémie.
Kľúčové slová:
ateroskleróza – aterogénna dyslipidémia – dysliporoteinémia – hypertriacylglycerolémie
Úvod
V súčasnosti sa manažmentu dyslipoproteinémie v rámci manažmentu kardiovaskulárnych ochorení, metabolických porúch a diabetes mellitus venujú rozličné odporučenia [1,2,3]. Za známy rizikový faktor je považovaný LDL-cholesterol, ktorý je aj cieľom režimových a liečebných opatrení. Avšak aterogénny lipidový profil je okrem vyššieho LDL-C tvorený aj hypertriacylglycerolémiou. Pre manažment hypertriacylglycerolémie platia rôzne národné a medzinárodné odporučenia. K existujúcim odporučeniam (Lipidový konsenzus 2, Odporučenie Európskej kardiologickej spoločnosti) pribudli koncom roku 2012 aj odporučenia Americkej endokrinologickej spoločnosti (The Endocrine Society – ES), ktoré tiež zdôrazňujú dôležitosť ovplyvnenia aj hladiny triacylglycerolov pri komplexnom manažmente pacienta s kardio-metabolickým rizikovým profilom.
Dyslipoproteinémie
Poruchy metabolizmu plazmatických lipidov a lipoproteínov (dyslipoproteinémie) predstavujú skupinu metabolických ochorení, charakterizovanú zvýšenou hladinou lipidov a lipoproteínov v plazme alebo ich nevhodným aterogénnym zložením. Jedná sa o poruchu syntézy alebo poruchu ich odbúravania. V súčasnosti sa považujú za jeden z najvýznamnejších rizikových faktorov kardiovaskulárnych ochorení (KVO) [4,5]. Existujú presvedčivé dôkazy o vzťahu hladiny LDL-cholesterolu (LDL-C) k tejto skupine ochorení, preto sa pozornosť hypolipidemickej liečby vo väčšej miere sústreďovala na dosiahnutie cieľových hladín celkového cholesterolu a LDL-C. V sledovaniach významu vzťahu hladiny triacylglycerolov (TG) a kardiovaskulárnych ochorení bolo viacero nejasností a niektoré aj v súčasnej dobe zostávajú predmetom ďalších skúmaní [1,4,5].
Vyšetrenie hladiny triacylglycerolov
V zhode s odporúčaniami the National Cholesterol Education Program (NCEP) a Expert Panel on Detection, Evaluation and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III-ATP III) sa odporúča u dospelej populácie vyšetrenie hladiny TG ako súčasť vyšetrenia lipidového spektra nalačno aspoň každých 5 rokov [6].
Podľa posledných odporúčaní pre manažment dyslipoproteinémií vydaných European Society of Cardiology (ESC) a European Atherosclerosis Society (EAS) sa má skríning vykonávať u mužov ≥ 40 rokov, u žien ≥ 50 rokov alebo v menopauze, a u všetkých pacientov bez ohľadu na vek s manifestnou aterosklerózou, diabetes mellitus 2. typu (DM2T), s pozitívnou rodinnou anamnézou včasnej aterosklerózy, s artériovou hypertenziou, s centrálnou obezitou, autoimunitnými systémovými ochoreniami, chronickou renálnou insuficienciou (GF < 60 ml/min/1,73m2), s klinickou manifestáciou dysliporpoteinémií (xantomatóza, xantelazmy, arcus lipoides corneae) [2].
Pokým mierny a stredný stupeň hypertriacylglycerolémie môže zvyšovať riziko KV-ochorení, ťažký a veľmi ťažký stupeň zvyšuje riziko pankreatitídy [7]. Rozdelenie hypertriacylglycerolémie nalačno podľa stupňa závažnosti (podľa NCEP ATP III a podľa ES uvádza tab. 1.
![Stupne hypertriacylglycerolémie nalačno podľa NCEP ATP III a Americkej endokrinologickej spoločnosti [1,8]](https://www.forumdiabetologicum.sk/media/cache/resolve/media_object_image_small/media/image/3af39f7dab7a44750a68d45674222428.png)
ES odporúča vyšetrovať sérovú hladinu TG v rámci lipidového profilu v stave nalačno [1]. Vyšetrenie nalačno poskytuje stabilnejšie koncentrácie ako i možnosť vypočítať hladinu LDL-C použitím Friedewaldovej rovnice [9]:
Podľa tejto rovnice sa dá LDL-C vypočítať, len ak hladina TG nepresiahne 4,5 mmol/l. U pacientov s hypertriacylglycerolémiou (HTG) sa neodporúča rutinné vyšetrenie lipoproteínových častíc typu apoB alebo Lp(a) [10]. Sérová hladina TG je vyššia u mužov a zvyšuje sa u oboch pohlaví s vekom. Často sprevádza iné metabolické abnormality spojené so zvýšeným kardiovaskulárnym rizikom. Faktory prispievajúce k zvýšenej hladine sérových TG sú nadváha, nízka fyzická aktivita, nadmerný príjem alkoholu, metabolický syndróm alebo diabetes mellitus, ako aj geneticky podmienené poruchy metabolizmu lipidov a lipoproteínov [11]. Nie zriedkavo je HTG výsledkom kombinácie genetických faktorov so súčasne zvýšenou tvorbou prípadne zníženým odbúravaním TG.
Primárne a sekundárne príčiny hypertriacylglycerolémie
Triacylglyceroly sú chemicky estery glycerolu a mastných kyselín. Pre ľudský organizmus sú dôležitým zdrojom energie. Tvoria hlavnú zložku lipidov prijatých v potrave. Pôsobením pankreatickej lipázy sa z triacyglycerolov odštiepujú mastné kyseliny. Vznikajú 2-monoacylglyceroly, ktoré sa formujú do micel. V centre micel sú monoacylglyceroly, cholesterol a mastné kyseliny, na povrchu micel konce žlčových kyselín a fosfolipidov. Z micel po kontakte s mikroklkmi čreva difundujú do enterocytu ich lipidové zložky. Resorbované mastné kyseliny sú v endoplazmatickom retikule resyntetizované na triacylglyceroly a súčasne využité na esterifikáciu cholesterolu. TG sa kompletizujú do lipoproteínových komplexov – chilomikrónov, ktoré sa exocytózou dostávajú do medzibunkových priestorov a odtiaľ sú prenášané lymfatickými cievami do krvi. Ďalším lipoproteínom, ktorý sa podieľa na transporte TG, sú VLDL-častice syntetizované v pečeni [1,3,5,8].
Všeobecne je hypertriacylglycerolémia spôsobená buď zvýšenou produkciou alebo zníženým katabolizmom, prípadne kombináciou oboch. Príkladom výskytu zvýšenej hladiny TG je metabolický syndróm a DM2T, ale aj nadváha so sedavým spôsobom života. Tieto podmieňujú inzulínovú rezistenciu s hyperinzulinémiou, ktorá má za následok zvýšenú de novo produkciu TG. Vplyv inzulínovej rezistencie na produkciu TG a VLDL je však u jednotlivcov veľmi variabilný.
Z hľadiska etiológie rozdeľujeme HTG na primárne, geneticky podmienené, a sekundárne, ktoré sú dôsledkom iného ochorenia, resp. jeho liečby. Pri zistení zvýšenej hladiny TG v stave nalačno, je preto nutné pred rozhodnutím o terapeutickom postupe vylúčiť sekundárnu príčinu. Najčastejšie príčiny HTG uvádza tab. 2.
![Najčastejšie príčinyHTG [1]](https://www.forumdiabetologicum.sk/media/cache/resolve/media_object_image_small/media/image/ecd8a76bd59896c1fc4b066fb906cef9.png)
Sekundárne príčiny
Vzhľadom na stimulujúcu funkciu estrogénov na produkciu lipoproteínov bohatých na TG v pečeni dochádza k zvýšeniu hladiny TG počas gravidity, pričom v 3. trimestri môžu hladiny prekročiť až dvojnásobok hodnoty pred graviditou. U žien s predchádzajúcou nadprodukciou TG môže takýto nárast výrazne zvýšiť riziko pankreatitídy s ohrozením života plodu. Perorálne estrogény podávané ako substitučná terapia alebo v antikoncepčných preparátoch zvyšujú hladinu TG zvyšovaním produkcie VLDL-častíc pečeňou. Tento efekt je menej významný pri transdermálnej aplikácii vzhľadom na nižšiu hepatálnu expozíciu. So zvýšenou hladinou TG sa stretávame takisto pri liečbe tamoxifenom, menej výrazný je efekt pri raloxifene [12,13].
Deficit hormónov štítnej žľazy je spojený so zvýšenou hladinou LDL-C, čo je spôsobené zníženou funkciou LDL-receptorov, tedy je sprevádzaný hypertriacylglycerolémiou. Obdobne stúpa hladina TG aj pri Cushingovom syndróme, či počas terapie glukokortikoidmi [14].
U pacientov s neliečeným diabetes mellitus, častejšie pri DM2T, sa bežne stretávame s hypertriacylglycerolémiou, pri správnej liečbe sa hladina TG znižuje. Mierna HTG, typická pre DM2T, býva spojená s centrálnou obezitou a inzulínovou rezistenciou [15,16].
Vrodené a dedičné lipodystrofie sú asociované so stredným až ťažkým stupňom HTG. Sú charakteristické stratou tukového tkaniva celkovo, alebo sú postihnuté len niektoré oblasti tela. Niektoré typy sa manisfestujú už v čase narodenia, iné v detstve alebo puberte. Dedičnosť týchto ochorení je autozomálne dominantná alebo recesívna. So získanou lipodystrofiou so zvýšenou hladinou TG sa možno stretnúť u HIV-pozitívnych pacientov liečených vysokými dávkami antiretrovirotík. Zvýšená hladina TG môže byť sprievodným znakom aj niektorých typov glykogenóz, autoimunitných ochorení (systémový lupus erythematodes), mnohopočetného myelómu, septických stavov (zvýšenou produkciou VLDL-častíc), hepatálnych a renálnych ochorení [1,17].
Na zvýšenej hladine TG sa môžu podieľať aj viaceré liečivá. Patria k nim tiazidové diuretiká, betablokátory (atenolol, metoprolol, menej karvedilol) a druhogeneračné antipsychotiká (klozapín, risperidon, olanzepín), ktoré bývajú asociované s väčším rizikom hmotnostného prírastku, inzulínovej rezistencie, a tým progresie metabolického syndrómu. Sekvestranty žlčových kyselín môžu zhoršiť HTG a sú kontraindikované u pacientov s TG nad 11,2 mmol/l [1,18].
Z návykových látok je najvýznamnejší alkohol, ktorý zvyšuje syntézu mastných kyselín a znižuje ich oxidáciu a má mierne stimulujúci účinok na hepatálnu sekréciu VLDL-častíc. Efekt alkoholu závisí od dávok, frekvencie a predchádzajúcich porúch metabolizmu lipidov [19].
Primárne príčiny
Familiárna kombinovaná hyperlipoproteinémia
Pri familiárnej kombinovanej hyperlipoproteinémii (FCHL) lipidový fenotyp varíruje od izolovanej hypertriacylglycerolémie po izolovanú hypercholestrerolémiu. U jedného jedinca sa môžu lipidové fenotypy v rôznom časovom období meniť. U pacientov nachádzame často zvýšené hladiny TG a LDL-C s prevahou malých denzných LDL-častíc a vysokú koncetráciu apoB. Vysoká hladina TG, a tým vysoká hladina voľných mastných kyselín, sa podieľajú na vzniku inzulínovej rezistencie, preto sa u týchto pacientov stretávame s metabolickým syndrómom až DM2T. Odhliadnuc od etiológie, kombinácia HTG a zvýšené hladiny LDL-C s prevahou malých denzných LDL-častíc sa javí podobne ako zvýšené riziko asociované so samostatne zvýšenou hladinou LDL-C [1,20].
Familiárna hypertriacylglycerolémia
Familiárna hypertriacylglycerolémia (FHTG) je dedičné ochorenie s autozomálne dominantným typom dedičnosti. Je charakterizované zvýšenou syntézou TG za prítomnosti VLDL-častíc s vysokým obsahom TG. Ochorenie sa prejavuje často, až kým nedosiahne stupeň veľmi ťažkej HTG, dovtedy bývajú postihnutí jedinci asymptomatickí. Javí sa, že FHTG nie je asociovaná so zvýšeným predčasným KV-rizikom. Prítomné je však zvýšené riziko prechodu do syndrómu chylomikronémie alebo prípadne pankreatitídy, najmä pokiaľ u jedinca nachádzame súčasne sekundárnu príčinu zvýšenej hladiny TG, ako napr. neliečený diabetes mellitus alebo užívanie rizikových liekov. Pri stanovení diagnózy sa riadime rodinnou anamnézou a vyšetrením profilu nalačno. Hladina TG sa pohybuje v rozpätí stredne ťažkého stupňa HTG, pričom postihuje priemerne polovicu prvostupňových príbuzných. V rodinnej anamnéze obyčajne nenachádzame údaje o predčasnom KV-riziku. Dôležité je odlíšiť FHTG, bez zjavného predčasného rizika KV-chorôb, od FCHL, pri ktorom je riziko vysoké. Problémom môžu byť prípady, kedy je pri FCHL súčasne vysoká hladina TG. Sprievodne zvýšená hladina apoB alebo LDL-C spolu s pozitívnou osobnou alebo rodinnou anamnézou môžu byť pomocným vodítkom k diagnóze FCHL [1,21].
Syndróm chylomikronémie
Syndróm chylomikronémie je asociovaný s rizikom pankreatitídy. Presný mechanizmus nie je známy, predpokladá sa nárazové uvoľnenie mastných kyselín a lyzolecitínu z chylomikrónov s prekročením kapacity albumínu v pankreatických kapilárach. Syndróm je spojený s bolesťami brucha, eruptívnymi xantómami v gluteálnej oblasti a nad extenzormi, prechodnými stratami pamäte. Pokiaľ sa nelieči, môže byť príčinou rekurentných pankreatitíd. Riziko pankreatitídy výrazne stúpa pri hladine TG nad 22,4 mmol/l, udržanie hladiny TG menej ako 11,2 mmol/l obyčajne postačuje ako prevencia recidív, resp. atakov akútnej pankreatitídy. Okrem medikamentóznej liečby je nutná reštrikcia tukov v strave [1,22].
Familiárna hypoalfalipoproteinémia
Familiárna hypoalfalipoproteinémia s vysokou hladinou TG je spojená u väčšiny jedincov so zníženou hladinou HDL-C, a tým zvýšeným predčasným KV-rizikom. V rámci diferenciálnej diagnostiky sa zamieňa s FHTG. Takmer všetky formy závažnejších vrodených foriem zníženého HDL-C sú spojené s miernym až stredným stupňom HTG (napr. deficit apoA-I, morbus Tangier) [1,23].
Dysbetalipoproteinémia
Pri dysbetalipoproteinémii je zvýšená hladina cholesterolu aj TG a vysoké predčasné KV-riziko, predispozične býva postihnutý periférny vaskulárny systém. Ku klinickým prejavom patrí tuberózna xantomatóza a oranžové tukové depozity v palmárnych ryhách, ktoré sú patognomické, avšak nie vždy prítomné [24].
Príčiny podmienené genetickou náchylnosťou
Hypertriacylglycerolémia je jedným z komponentov metabolického syndrómu. Definícia metabolického syndrómu vychádza z konsenzu the National Heart, Lung, and Blood Institute, the International Diabetes Federatin, a the American Heart Association (IDF-AHA/NHBLI 2009), uvádza ju tab. 3. Podmienkou stanovenia diagnózy metabolického syndrómu je splnenie aspoň 3 z 5 kritérií [25,26].
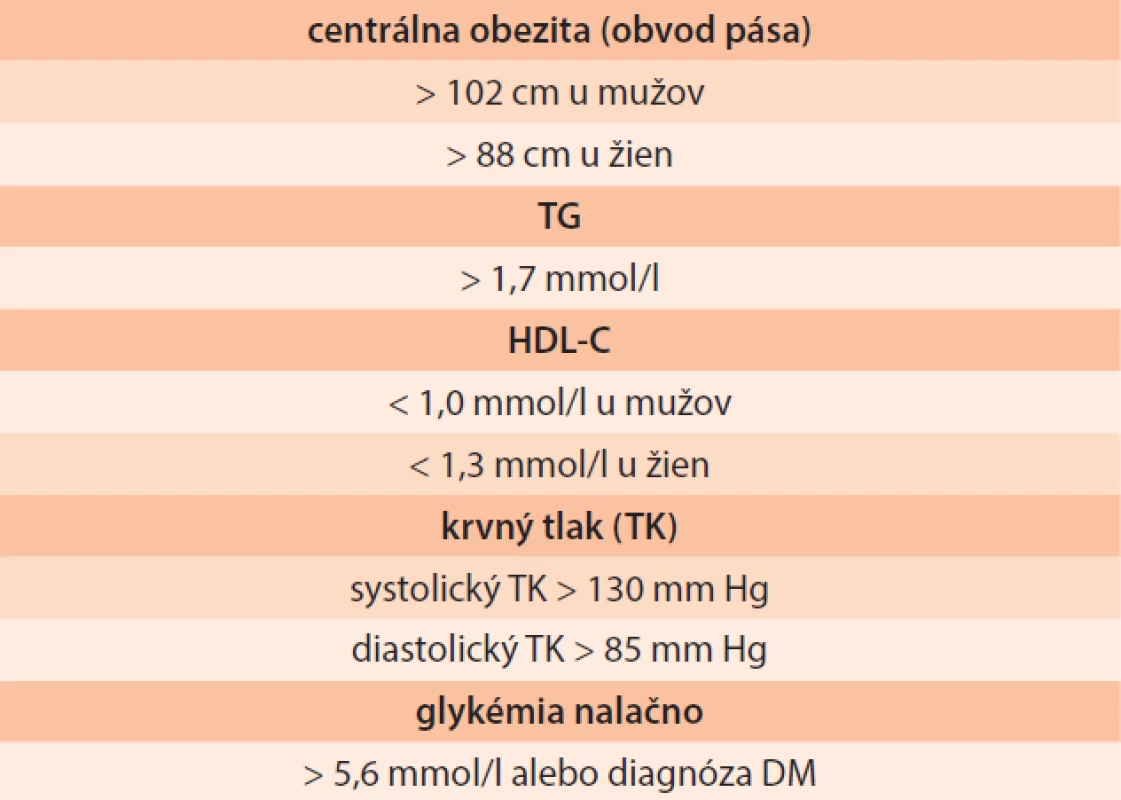
Súčasťou ochorení asociovaných so zvýšeným KV-rizikom je často zvýšená hladina TG. Typickým príkladom je DM2T, metabolický syndróm alebo vrodené formy HTG so súčasne zníženou hladinou HDL-C a zvýšeným množstvom malých denzných LDL-častíc. Zvýšená sérová hladina TG však môže byť v niektorých prípadoch hodnotená skôr ako marker pre KV-riziko, a nie ako kauzálny faktor. Neexistuje lineárna závislosť medzi hladinou TG a KV-ochoreniami. Ako bolo spomenuté, pacienti s FHTG, ktorá je v bežnej populácii zastúpená relatívne častejšie, nemajú zvýšené predčasné KV-riziko. Veľké lipoproteíny bohaté na TG nie sú aterogénne, pokiaľ sú dostatočne veľké na to, aby penetrovali do stien artérií. Práve cholesterol má výrazný podieľ na patogenéze aterosklerotických zmien, avšak zvýšená lipolýza lipoproteínov bohatých na TG môže viesť k zvýšenej permeabilite ciev s jej súčasnou infiltráciou LDL-časticami. V súčasnosti, vzhľadom na nedostatok jasných dôkazov o zníženom KV-riziku pri znižovaní hladiny TG, sa hypertriacylglyceridémia hodnotí ako rizikový faktor len u vybraných jedincov.
ES u pacientov s primárnou hypertriacylglycerolémiou odporúča zhodnotiť ostatné kardiovaskulárne rizikové faktory, ako je centrálna obezita, artériová hypertenzia, poruchy metabolizmu sacharidov, fajčenie atď [1].
Manažment hypertriacylglyceridémie
Nefarmakologická liečba
ES odporúča pri miernom až strednom stupni hypertriacylglycerolémie ako iniciálnu terapiu zmenu stravovacích návykov, zvýšenie pohybovej aktivity a redukciu hmotnosti u jedincov s nadváhou alebo obezitou [1].
Úprava stravovacích návykov
Práve hmotnostný prírastok, nedostatok pohybu a strava bohatá na jednoduché cukry a sladené potraviny sú častou príčinou zvýšenej hladiny TG ako u dospelých, tak aj mladistvých. Znížený príjem sacharidov v strave viedol k zníženiu hladiny TG nalačno. Zistilo sa, že fruktóza obsiahnutá v sladených potravinách zvyšovala hladiny TG výraznejšie v porovnaní s glukózou, preto sa odporúča znížiť príjem sladených potravín (vysoký podiel fruktózy). Pre koreláciu glykemického indexu s rýchlosťou vzostupu TG po príjme potravy s obsahom sacharidov sa odporúča preferovať potraviny s nízkym glykemickým indexom. Odporúča sa redukcia príjmu nasýtených mastných kyselín a preferencia nenasýtených mastných kyselín. Príjem tukov by mal tvoriť 25–30 % z celkového denného energetického príjmu. U pacientov s nadváhou alebo obezitou je nutné pre redukciu hmotnosti celkovo znížiť denný kalorický príjem [1,27].
Pohybový režim
Pozorovalo sa, že vplyvom cvičenia deň pred príjmom jedla s vysokým obsahom tukov, bol postprandiálny vzostup TG menej výrazný. Mechanizmus nie je jasný a benefit cvičení je v týchto prípadoch relatívne krátkodobý. Rozsah pohybovej aktivity podmieňujúci tento efekt nebol stanovený, ale aeróbny typ cvičenia alebo odporové cvičenie miernej intenzity v trvaní 30–60 minút bolo efektívne z hľadiska zníženia hladiny TG. Porovnávaním pohybových programov v zmysle aeróbnych programov s programami s vysokointenzívnym cvičením sa zistilo, že intenzívne programy mali mierne vyšší efekt na zvyšovanie HDL-C, avšak menší na redukciu hladiny TG, celkového ako i LDL-C. Ďalšie sledovania priniesli zistenie, že najefektívnejšia je kombinácia aeróbneho cvičenia s miernymi odporovými cvičeniami v porovnaní s čisto aeróbnym cvičením. Redukcia hmotnosti v prípade nadváhy alebo obezity je kauzálnou v snahe redukovať hladinu TG [1,28].
Farmakologická liečba
ES odporúča pri ťažkom a veľmi ťažkom stupni hypertriacylglycerolémie za účelom redukcie rizika pankreatitídy znížený príjem tukov a jednoduchých sacharidov v kombinácii s farmakologickou liečbou [1].
ES ďalej odporúča pre pacientov so stredným stupňom hypertriacylglycerolémie cieľové hodnoty hladiny non–HDL-C v zhode s odporúčaniami NCEP ATP [1,8]. Non-HDL cholesterol (celkový cholesterol/TC mínus HDL-C) odráža podiel cholesterolu vo všetkých aterogénnych lipoproteínoch. Sledovanie hladiny HDL-C je odporúčané u jedincov s hypertriacylglycerolémiou jednak pre stratifikáciu rizika a jednak pre sekundárny terapeutický cieľ. Možnou alternatívou je zhodnotenie koncentrácie apoB. Keďže na povrchu každej častice chylomikrónu, VLDL, IDL, LDL a Lp(a) je prezentovaná jedna molekula apoB, existuje dobrá korelácia medzi hladinou apoB a non-HDL-C. Koncentrácia apoB tak odráža koncentráciu aterogénnych lipoproteínových častíc. Keďže koncentrácia apoB môže pomôcť pri odlíšení FCHL od FHTG, môže byť vyšetrenie apoB pri úvodnom hodnotení hypertriacylglycerolémie prínosom.
ES odporúča použitie fibrátov ako lieku prvej voľby na zníženie hladiny TG u pacientov s rizikom TG-indukovanej pankreatitídy [1].
ES navrhuje, aby sa skupiny liečiv (fibráty, niacín, omega-3 polynenasýtené mastné kyseliny) samostatne alebo v kombinácii so statínmi považovali za možnosť liečby u pacientov so stredným až ťažkým stupňom HTG [1].
Fibráty
Terapia fibrátmi by sa mala jednoznačne zvážiť u pacientov s ťažkým a veľmi ťažkým stupňom HTG a zvážiť u pacientov so stredným stupňom HTG. Fibráty znižujú hladinu TG o 30–50 % a niekedy môžu zvýšiť hladinu HDL-C. U pacientov s vysokou hladinou TG môžu spôsobiť zvýšenie hladiny LDL-C, pokým u miernejších foriem hladinu LDL-C znížujú. U pacientov s pankreatitídou indukovanou TG je benefitnou sprievodná liečba fibrátmi na udržanie hladiny TG pod 22,4 mmol/l ako prevencia rekurencie ochorenia. Odporúčanou cieľovou hodnotou liečby je hladina pod 11,2 mmol/l. Pri veľmi ťažkom stupni hypertriacylglycerolémie s pankreatitídou sa neodporúča liečba infúziami heparínu ani plazmaferézou. Doterajšie štúdie neukázali celkový benefit fibrátov na pokles kardiovaskulárnej ani celkovej mortality. Analýzy štúdií ukázali, že použitie fibrátov u pacientov so stredným stupňom HTG viedli k zníženiu združených KV-príhod, ale neznížili mortalitu. Ukázali tiež, že liečba pacientov s hladinou TG nižšou ako 2,3 mmol/l neprináša benefit. Fibráty sú všeobecne dobre tolerované. Vedľajšie účinky zahŕňajú gastrointestinálny diskomfort, možný je zvýšený výskyt cholesterolových žlčových kameňov. Sú kontraindikované u pacientov s chorobami pečene a žlčníka. Primárne sa vylučujú obličkami, preto treba zvýšiť opatrnosť pri pacientoch s renálnou insuficienciou. Fenofibrat je pre menšie riziko myopatie preferovaným fibrátom do kombinácie so statínom. Pre možnosť interakcie u pacientov liečených warfarinom je nutný častejší monitoring INR [1,29,30].
Niacín
Niacín (kyselina nikotínová a jej deriváty) vedie k zníženiu hladín LDL-C, TG a k zvýšeniu hladiny HDL-C. V dávke 500–2 000 mg znižuje hladinu TG o 10–30 %, zvyšuje HDL o 10–40 % a znižuje LDL-C o 5–20 %. Najčastejší vedľajší účinok je kožný flush, čo je spôsobené uvoľňovaním prostaglandínu D2 z buniek kože, ktorý vedie k vazodilatácii. Objavuje sa asi 15–60 minút po užití lieku. Užitie po jedle znižuje výskyt flushu.Z nežiadúcich účinkov je najvážnejším hepatotoxicita, ďalej porucha, prípadne zhoršenie glukózovej tolerancie a hyperurikémia. Je kontraindikovaný u pacientov s aktívnou vredovou chorobou gastroduodena [1,31].
Na Slovensku bola donedávna kyselina nikotínová súčasťou kombinovaného prípravku s laropiprantom. V januári 2013 bola registrácia prípravku dočasne pozastavená a liečba ukončená, keďže predbežné výsledky preukázali, že prínos liečby týmto prípravkom neprevyšuje jeho riziká (podľa výzvy ŠUKL zverejnenej na číselníku ADC).
Omega-3-polynenasýtené mastné kyseliny(PUFA)
Medzi PUFA patria kyselina eikozapentaénová (EPA) a dokozahexaénová (DHA). Ich zdrojom je rybí tuk. Znižujú hladinu TG nalačno aj postprandiálne. Priemerne 3–4 g/deň EPA + DHA je dávka potrebná na redukciu hladiny TG o 20–50 %. Mierne, približne o 5 %, zvyšujú hladinu HDL-C. Doteraz žiadne štúdie s vysokými dávkami PUFA u pacientov s hypertriacylglycerolémiou nepreukázali benefit na kardiovaskulárne výsledky. Túto liečbu možno zvážiť u pacientov so zvýšenou hladinou TG pri hladinách nad 11,2 mmol/l. Z vedľajších účinkov sa pri vysokých dávkach vyskytuje pachuť po rybách a nadmerné grganie [1,32].
Statíny
ES odporúča nepoužívať statíny v monoterapii u pacientov s ťažkým a veľmi ťažkým stupňom HTG. Statíny môžu byť prínosom v liečbe HTG stredného stupňa v indikácii modifikácie KV-rizika. Statíny znižujú hladinu TG priemerne o 10–15 % v závislosti od dávky. Vysoké dávky statínov, ako 80 mg atorvastatínu alebo 40 mg rosuvastatínu, môžu znížiť hladinu TG o 25–30 %. Monoterapia statínmi by nemala byť liečbou v prvej línii na zníženie hladiny TG u pacientov s hodnotami TG nad 11,2 mmol/l. Nežiadúce účinky sa prejavujú u 5–10 % pacientov. Svalové kŕče, bolesti svalov až po únavu sa objavujú asi u 10 % pacientov, rabdomyolýza je zriedkavá. Podmienky predisponjúce k ťažkej myopatii sú vyšší vek, renálna insuficiencia, akútne ochorenie a užívanie väčšieho množstva liekov [1,2,3,5].
Kombinovaná liečba
Vzhľadom na jednotlivé liečivá uvedené vyššie a ich odlišné mechanizmy znižovania hladiny TG, je možnosť po dôkladnej úvahe a zhodnotení možných interakcií pristúpiť aj ku kombinovanej liečbe [1,33].
MUDr. Peter Jackuliak
peter.jackuliak@gmail.com
MUDr. Miriam Avramovová
prof. MUDr. Juraj Payer, CSc.
V. interná klinika LF UK a UNB, Nemocnice Ružinov, Bratislava
www.fnspba.sk/Nemocnica-Ruzinov/
Doručené do redakcie 9. mája 2013
Prijaté do tlače po recenzii 21. mája 2013
Zdroje
1. Berglund L, Brunzell JD, Goldberg AC (eds) et al (Endocrine society). Evaluation and Treatment of Hypertriglyceridemia: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2012; 97(9): 2969–2989.
2. Reiner Z, Catapano AL, De Backer G (eds) et al (European Association for Cardiovascular Prevention & Rehabilitation). ESC/EAS Guidelines for the management of dyslipidaemias. The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS). Eur Heart J 2011; 32(14): 1769–1818.
3. Filipová S, Mikeš Z, Dukát A et al. Aktualizácia lipidového konsenzu-2. Cardiol 2006; 15(6): 313–316.
4. Krahulec B. Obezita a niektoré faktory prostredia podporujúce vznik metabolického syndrómu. Cardiol 2005; 14(4): 161–165.
5. Fábryová Ľ. Manažment aterogénnej dyslipidémie pri metabolickom syndróme. Via pract 2007; 4(Suppl 4): 13–18.
6. Atkins D, Best D, Briss PA et al. Grading quality of evidence and strength of recommendations. BMJ 2004; 328(7454): 1490–1497.
7. Murad MH, Hazem A, Coto-Yglesias F et al. The association of hypertriglyceridemia with cardiovascular events and pancreatitis: a systematic review and meta-analysis. BMC endocr disord 2012; 12.2. Dostupné z DOI: <http://doi:10.1186/1472–6823–12–2>.
8. Alexander CM, Landsman PB, Teutsch SM, Haffner SM. Third National Health and Nutrition Examination Survey (NHANES III); National Cholesterol Education Program (NCEP). NCEP-defined metabolic syndrome, diabetes, and prevalence of coronary heart disease among NHANES III participants age 50 years and older. Diabetes 2003; 52(2): 1210–1214.
9. Sniderman AD, Blank D, Zakarian R et al. Triglycerides and small dense LDL: the twin Achilles heels of the Friedewald formula. Clin Biochem 2003; 36(7): 499–504.
10. Swiglo BA, Murad MH, Schünemann HJ et al. A case for clarity, consistency, and helpfulness: state-of-the-art clinical practice guidelines in endocrinology using the grading of recommendations, assessment, development, and evaluation system. J Clin Endocrinol Metab 2008; 93(3):666–673.
11. Mora S, Rifai N, Buring JE, Ridker PM. Fasting compared with nonfasting lipids and apolipoproteins for predicting incident cardiovascular events. Circulation 2008; 118(10): 993–1001.
12. Sanderson SL, Iverius PH, Wilson DE. Successful hyperlipemic pregnancy. JAMA 1991; 265(14): 1858–1860.
13. Carr MC, Knopp RH, Brunzell JD et al. Effect of raloxifene on serum triglycerides in women with a history of hypertriglyceridemia while on oral estrogen therapy. Diabetes Care 2005; 28(7):1555–1561.
14. Retnakaran R, Connelly PW, Goguen J. Unmasking of type III hyperlipoproteinemia by hypothyroidism: a dramatic illustration of altered lipoprotein metabolism in a postpartum woman. Endocr Pract 2005; 11(6): 394–398.
15. Brunzell JD, Ayyobi AF. Dyslipidemia in the metabolic syndrome and type 2 diabetes mellitus. Am J Med 2003; 115 (Suppl 8a):24s-28s.
16. Alberti KG, Zimmet P, Shaw J (for the Epidemiology task force Consensus Group). The metabolic syndrome – a new worldwide definition. Lancet 2005; 366(9491): 1059–1062.
17. Garg A, Agarwal AK. Lipodystrophies: disorders of adipose tissue biology. Biochim Biophys Acta 2009; 1791(6): 507–513.
18. Stone NJ. Secondary causes of hyperlipidemia. Med Clin North Am 1994; 78(1):117–141.
19. Brinton EA. Effects of ethanol intake on lipoproteins and atherosclerosis. Curr Opin Lipidol 2010; 21(4): 346–351.
20. Veerkamp MJ, de Graaf J, Hendriks JC et al. Nomogram to diagnose familial combined hyperlipidemia on the basis of results of a five-year follow-up study. Circulation 2004; 109(24): 2980–2985.
21. Austin MA, McKnight B, Edwards KL et al. Cardiovascular disease mortality in familial forms of hypertriglyceridemia: a 20-year prospective study. Circulation 2000; 101: 2777–2782.
22. Brunzell JD, Deeb SS. Familial lipoprotein lipase deficiency, apoC-II deficiency, and hepatic lipase deficiency. In: Scriver CR, Beaudet Al, Sly Ws, Valle D (eds). The metabolic basis of inherited disease. 8th ed. McGraw-Hill: New York 2001: 2789–2816.
23. Genest Jr J, Bard JM, Fruchart JC et al. Familial hypoalphalipoproteinemia in premature coronary artery disease. Arterioscler Thromb 1993; 13(12):1728–1737.
24. Mahley RW, Huang Y, Rall Jr SC. Pathogenesis of type III hyperlipoproteinemia (dysbetalipoproteinemia). Questions, quandaries, and paradoxes. J Lipid Res 1999; 40(11): 1933–1949.
25. Grundy SM, Cleeman JL, Daniels SR (eds) et al (American Heart Association; National Heart, Lung, and Blood Institute). Diagnosis and management of the metabolic syndrome. An American Heart Association/National Heart, Lung and Blood Institute Scientific Statement. Circulation 2005; 112(17): 2735–2752.
26. Kassi E, Pervanidou P, Kaltsas G, Chrousos G. Metabolic syndrome: definitions and controversies. BMC Med 2011; 9:48. Dostupné z DOI: <http://doi:10.1186/1741–7015–9-48>.
27. Mensink RP, Zock PL, Kester AD, Katan MB. Effects of dietary fatty acids and carbohydrates on the ratio of serum total to HDL cholesterol and on serum lipids and apolipoproteins: a meta-analysis of 60 controlled trials. Am J Clin Nutr 2003; 77(5): 1146–1155.
28. Graham TE. Exercise, postprandial triacylglyceridemia, and cardiovascular disease risk. Can J Appl Physiol 2004; 29(6): 781–799.
29. The BIP Study Group 2000 secondary prevention by raising Hdl cholesterol and reducing triglycerides in patients with coronary artery disease: the Bezafibrate infarction Prevention (BIP) study. Circulation 2000; 102(1): 21–27.
30. Keech A, Simes RJ, Barter P et al. Effects of long-term fenofibrate therapy on cardiovascular events in 9,795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial. Lancet 2005; 366(9500): 1849–1861.
31. Brown BG, Zhao XQ, Chait A et al. Simvastatin and niacin, antioxidant vitamins, or the combination for the prevention of coronary disease. N Engl J Med 2001; 345(22): 1583–1592.
32. Hu FB, Bronner L, Willett WC et al. Fish and omega-3 fatty acid intake and risk for coronary heart disease in women. JAMA 2002; 287(14): 1815–1821.
33. Sharma M, Ansari MT, Abou-Setta AM et al. Systematic review: comparative effectiveness and harms of combination therapy and monotherapy for dyslipidemia. Ann Intern Med 2009; 151(9): 622–630.
Štítky
Diabetologie Endokrinologie Interní lékařstvíČlánek vyšel v časopise
Forum Diabetologicum

2013 Číslo 2
Nejčtenější v tomto čísle
- Diabetická neuropatia: klinický obraz a súčasné možnosti diagnostiky a liečby
- Manažment hypertriacylglycerolémie z pohľadu najnovších odporúčaní Americkej endokrinologickej spoločnosti (The Endocrine Society)
- Diabetická nefropatia: epidemiológia a diagnostika
- Diabetická noha: epidemiologické údaje a aktuálne možnosti lokálnej liečby

