Liečba diabetes mellitus 1. typu pomocou inzulínovej pumpy – komu a prečo?
Insulin pump treatment in type 1 diabetes mellitus – for whom and why?
Insulin pump treatment, also known as continuous subcutaneous insulin infusion (CSII), is an important part of the diabetes mellitus (DM) treatment portfolio. This is an effective and flexible method of administering insulin that, when properly indicated and managed, generally leads to improved glycemic compensation and variability, reduction of GHbA1 (glycosylated hemoglobin), reduced frequency of severe hypoglycemia, correction of „dawn“ or „dark“ phenomena, reduction of „unawareness hypoglycemia“ syndrome, but also leads to the reduction of the total insulin dose compared to multiple daily injections (MDI), also contributes to improving the quality of life of diabetic patients.
Keywords:
continuous subcutaneous insulin infusion – multiple daily injections
Authors:
Dana Prídavková; Veronika Sváková; Udovít Šutarík; Marián Mokáň
Authors‘ workplace:
I. interná klinika Jesseniovej LF UK a UNM, Martin
Published in:
Forum Diab 2019; 8(2): 139-146
Category:
Review Article
Overview
Liečba inzulínovou pumpou, tiež známa ako kontinuálna subkutánna inzulínová infúzia (continuous subcutaneous insulin infusion – CSII) je dôležitou súčasťou liečebného portfólia diabetes mellitus (DM). Ide o efektívnu a flexibilnú metódu podávania inzulínu, ktorá pri správnej indikácii a manažmente spravidla vedie k zlepšeniu glykemickej kompenzácie a variability, redukcii GHbA1 (glykozylovaný hemoglobín), k zníženiu frekvencie výskytu závažnej hypoglykémie, korekcii „dawn“, či „dark“ fenoménu, k redukcii syndrómu „neuvedomenia si hypoglykémie“, ale aj k zníženiu celkovej dávky inzulínu v porovnaní s režimom mnohopočetných denných injekcií (multiple daily injections – MDI). V neposlednej miere prispieva aj k zlepšeniu kvality života pacientov s diabetom.
Klíčová slova:
kontinuálna subkutánna inzulínová infúzia – mnohopočetné denné injekcie
Úvod
Liečba inzulínom predstavuje základný stavebný kameň liečby pacientov s ochorením diabetes mellitus 1. typu (DM1T), ako ochorenia s progresívnou deštrukciou B-buniek pankreasu vedúcej k absolútnemu deficitu inzulínu. V našich podmienkach nemáme k dispozícii sofistikovanejšie zariadenie, ktoré by napodobňovalo fyziologickú sekréciu inzulínu, ako je tomu v prípade inzulínovej pumpy. Liečba DM1T prostredníctvom kontinuálnej subkutánnej inzulínovej infúzie (continuous subcutaneous insulin infusion – CSII) sa považuje za „zlatý štandard“ liečby [1].
Prototyp CSII bol predstavený v 60. rokoch 20. storočia v Los Angeles dr. Arnoldom Kadishom [2] a od uvedenia tejto liečby na trh pred viac ako 40 rokmi sa jej vývoj neustále zdokonaľuje. V súčasnej dobe expandujúcich technických vymožeností predchodcu dnešných inzulínových púmp (IP) ako je napr. prototyp Mill Hill s dvoma bazálnymi rýchlosťami (pomalou 47 μl/hod a rýchlou 375 μl/hod) so 17 minút trvajúcim návratom k východiskovej rýchlosti, vnímame ako veterána, ktorý napriek obmedzeným technickým parametrom oproti dnešnej dobe, dokázal ponúknuť výsledky vo forme zlepšenia glykemickej kontroly, a u väčšiny pacientov aj bez výskytu závažnej hypoglykémie [3]. V kontraste s históriou dnešné inzulínové pumpy poskytujú oveľa väčší komfort, viac technických možností, ktoré umožňujú flexibilitu, individualizáciu dávkovania inzulínu podľa typu aktivít, zdravotného stavu a v neposlednej miere niektoré vedia ochrániť pred vznikom hypoglykémie v súčinnosti s kontinuálnym glykemickým monitoringom (Continuous Glucose Monitoring – CGM). Takýto komfort poskytuje inzulínová pumpa Medtronic 640G.
Napriek vymoženostiam a rastúcemu počtu užívateľov CSII, hlavne u pediatrických pacientov existuje v európskych krajinách pomerne široká variabilita v ich používaní, pričom dáta ukazujú, že Európa zaostáva v akceptácii tejto technológie za Spojenými štátmi [4]. Na Slovensku, ako v jednej z mála krajín, je CSII s príslušenstvom uhrádzaná zdravotnou poisťovňou, a to v plnej výške v zmysle platných indikačných obmedzení, čo umožňuje využívať tento typ liečby v širšom meradle. Pomerne veľkoryso nastavené podmienky pre túto liečbu však nie sú dostupné vo všetkých krajinách, napr. v Maďarsku a Poľsku je liečba IP uhrádzaná v plnom rozsahu len u detí do 18 rokov [5]. V grafe 1 je znázornené používanie inzulínových púmp v Európe.
![Využívanie CSII u pacientov s DM1T v európskych krajinách. Upravené podľa [6]](https://pl-master.mdcdn.cz/media/image_pdf/86ae765869050bd08bf1ddd193f226f1.png?version=1566996034)
Hlavnou výhodou liečby prostredníctvom CSII je kontinuálne podávanie inzulínu v minimálnych dávkach. Podávanie mikrodávok inzulínu ale nie je u všetkých typov IP identické. Napr. u IP spoločnosti Medtronic frekvencia podávania závisí od aktuálnej hodinovej bazálnej dávky. Čím je hodinová bazálna dávka vyššia, tým je podávanie inzulínu častejšie, napr. pri rýchlosti 0,1 IU/hod sa podajú 4 dávky za hodinu (každých 15 minút), pri rýchlosti 1,0 IU/hod sa podá až 40 dávok inzulínu za hodinu (t. j. každých 90 sekúnd). Aj keď sa inzulín podáva podkožne a nie je primárne doručený do portálneho obehu, ako je tomu za fyziologických okolností, liečba inzulínovou pumpou predstavuje v súčasnosti alternatívu dostupnosti inzulínu najviac priblíženú jeho dostupnosti u zdravých jedincov. Individuálne dávkovanie umožňuje prispôsobiť sa metabolickým odchýlkam a zvyklostiam pacienta aj s ohľadom na pridružené komorbidity. Ďalšou praktickou výhodou je využitie dočasnej zmeny bazálnej dávky, teda dočasného navýšenia, alebo zníženia bazálnej hodinovej dávky inzulínu, podľa toho ako to činnosti, alebo stav pacienta vyžaduje (napr. fyzická aktivita, akútne ochorenie, operačný zákrok a pod) bez nutnosti opakovania korekčných bolusov a rizika sumácie účinku inzulínu. Nespornou výhodou je menší počet vpichov oproti MDI (Multiple Daily insulin Injections) -režimu (10–12/mesiac oproti 120–150/mesiac), čo nie je zanedbateľný fakt s ohľadom na lipodegeneráciu podkožia.
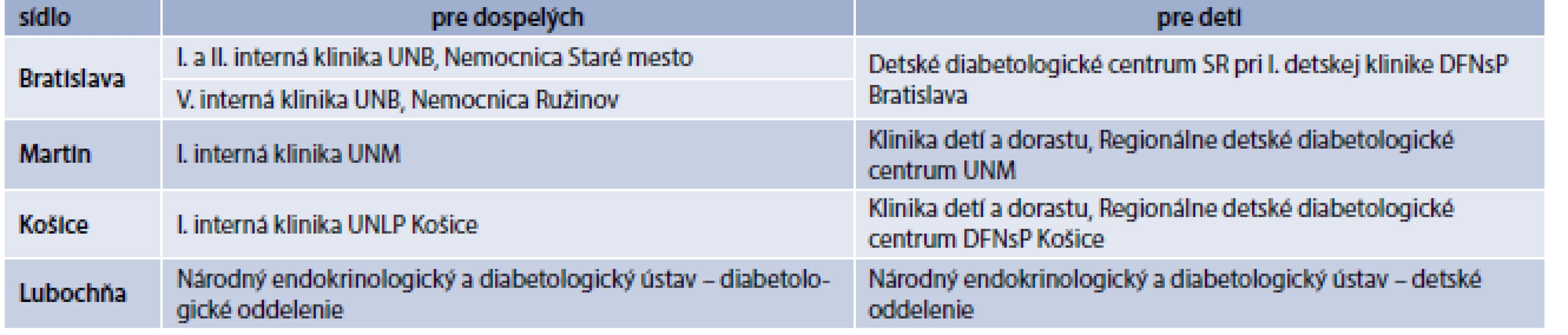
Elementárnym faktom úspešnej liečby CSII však ostáva správny výber pacienta, ktorý bude z liečby dlhodobo profitovať. Aktuálne platné kritériá a indikačné obmedzenia (schéma) umožňujú poskytnúť tento typ liečby väčšiemu spektru pacientov, ktorí sú liečení intenzifikovaným inzulínovým režimom vrátane bazálneho analógu. Liečbu pre dospelých môže navrhnúť lekár špecializácie diabetológia, poruchy látkovej premeny a výživy formou návrhu na liečbu inzulínovou pumpou alebo formou žiadosti o „zváženie“ tejto liečby pri odoslaní pacienta do Centra pre inzulínové pumpy. Liečbu môže po konzultácii s pacientom navrhnúť aj lekár Centra pre inzulínové pumpy (tab. 1) ideálne však so súhlasom ošetrujúceho diabetológa, pričom je potrebné rešpektovať indikačné obmedzenia [7].
![Schéma | Kritériá a indikačné obmedzenia pre liečbu inzulínovou pumpou. Upravené podľa [7]](https://pl-master.mdcdn.cz/media/image_pdf/617a4c2db473bc7e9110d8cba42dcd44.png?version=1566996064)
Indikácie a kontraindikácie liečby inzulínovou pumpou
Hypoglykémie
Pri tejto indikácii musí byť splnená požiadavka najmenej troch dokumentovaných hypoglykémií < 2,8 mmol/l za mesiac, alebo viac ako 1 ťažká hypoglykémia v priebehu posledných 3 mesiacov, alebo syndróm „neuvedomenia si hypoglykémie“, alebo nespoznané asymptomatické hypoglykémie odhalené pomocou kontinuálneho monitoringu glykémií. Vhodnosť tejto indikácie je pri hypoglykémiách, ktoré vedú k výrazným kontraregulačným osciláciám a labilite: pri syndróme „neuvedomovania si hypoglykémie“, pri hypoglykémiách pri vysokej citlivosti organizmu na zmeny dávok inzulínu, čo významne sťažuje titráciu dávok inzulínu (pri vysokej citlivosti organizmu na fyzickú aktivitu, pri chronických poruchách trávenia), či poruchách kontraregulačných mechanizmov (endokrinné poruchy).
Hyperglykémie s GHbA1 > 8,0 % DCCT
Na liečbu IP môžu byť indikovaní nedostatočne kompenzovaní pacienti napriek použitiu inzulínového analógu v trvaní najmenej 6 mesiacov. Táto indikácia vyžaduje opakované (najmenej 2-krát v týždni) významné vzostupy glykémie ráno pred raňajkami alebo pred večerou alebo počas noci > 10 mmol/l (zaznamenané v denníku pacienta). Efekt liečby musí byť potvrdený pomocou predošlého odskúšania servisnou pumpou.
Variabilita glykémií
Ďalšou indikáciou je variabilita glykémií napriek použitiu inzulínového analógu v trvaní minimálne 6 mesiacov. Ide o opakované (minimálne 1-krát v týždni 2 týždne po sebe, alebo 3-krát za mesiac) výrazné vnútrodenné oscilácie glykémií presahujúce rozmedzie 3,5–13,0 mmol/l, alebo variabilitu bazálnych glykémií (medzidenné variácie glykémie nalačno alebo pred večerou presahujúce rozmedzie 4–9 mmol/l).
Potreba dosiahnutia veľmi tesnej glykemickej kontroly bez rizika hypoglykémie a oscilácií glykémie
Medzi klinické situácie, ktoré favorizujú túto indikáciu je tehotenstvo, príprava na otehotnenie, stavy po transplantácii orgánov, stavy so zvýšeným mortalitným rizikom (pacienti, ktorí prekonali kardiovaskulárnu príhodu alebo cievnu mozgovú príhodu), predčasný výskyt diabetickej retinopatie alebo nefropatie alebo ťažkej neuropatie s klinickými prejavmi (bolesť) alebo následkami (diabetická noha) po menej ako 5 rokoch trvania DM alebo rýchlej progresie komplikácií [7].
Marginálne indikácie liečby CSII
Patrí sem napr. alergia na inzulín, u ktorej predstavuje liečba CSII „zlatý štandard“. CSII indukuje desenzitizáciu s dokázanou účinnosťou u pacientov s DM1T alebo DM2T, ktorí sú alergickí na všetky typy inzulínu alebo len na špecifický typ [8]. Patria sem aj lipoatrofické zmeny podkožia, pri ktorých CSII vplýva na minimalizovane opakovanej mikrotraumatizácie podkožia. Môže ísť aj o pacientov s veľmi nízkymi dávkami inzulínu (< 20 IU/deň) [8]. Možno sem zaradiť, bolesť alebo fóbiu z injekcií, ktoré môžu pomôcť rozhodnutiu pre túto liečbu.
Kontraindikácie
Aj keď absolútne kontraindikácie liečby CSII nie sú známe [7], literatúra zmieňuje ako kontraindikáciu závažné psychiatrické ochorenia, rýchlo progredujúce ischemické alebo proliferatívne retinopatie, u ktorých sa za škodlivú považuje liečba rapídne normalizujúca glykémie pred fotokoagulačnou liečbou laserom, je to aj život v extrémnych podmienkach z profesijných alebo osobných dôvodov – ako je teplo alebo zima, ktoré môžu viesť k inaktivácii inzulínu; profesionálne alebo športové potápanie, expozícia silnému elektromagnetickému poľu, ktorá môže spustiť nadlimitné dávkovanie inzulínu [8]. Za kontraindikáciu sa považuje aj nedostupnosť najmenej jedného školeného edukátora. Väčšina pacientov je primerane edukovaná a mentálne vybavená tak, že nevyžaduje prítomnosť odborného dohľadu vo väčšine prípadov. U časti pacientov hlavne v prvých 2–3 mesiacoch po nastavení sa vyžaduje dostupnosť aspoň 1 edukátora na asistenciu pri plnení zásobníka, zavádzaní kanyly a získavaní skúseností vo využívaní aj pokročilých funkcií pumpy. Za mandatórne sa považuje absolvovanie výcvikových sedení [2].
Relatívne kontraindikácie
Na strane pacienta môže ísť o nedostatočnú spoluprácu pri absolvovaní ambulantných kontrol, monitoringu glykémií alebo testovania na ketonúriu. Tieto kontraindikácie je potrebné prediskutovať s každým pacientom. Pokiaľ je k liečbe CSII pacient indikovaný, ale slabo angažovaný, mal by byť manažovaný multidisplinárnym tímom [8]. Relatívnou kontraindikáciou sú aj prípady, u ktorých dôvodom neuspokojivej kompenzácie je iná príčina, než sú nedostatky v dynamike účinku a vstrebávania inzulínu. Takými sú poruchy trávenia, zápalové ochorenia, endokrinopatie a pod, u ktorých je potrebné riešiť najskôr základné ochorenie. Úvahu o vhodnosti liečby pomocou IP vyžadujú aj situácie s častým výskytom diabetickej ketoacidózy a zápalovými ochoreniami kože. Riziko diabetickej ketoacidózy môže byť v niektorých prípadoch dokonca zvýšené [7]. Medzi relatívne prekážky zavedenia CSII patrí aj nedostatočná osobná hygiena s kolonizáciou kože stafylokokmi, terminálne štádium obličkového zlyhania, „end-stage kidney“ pre riziko vzniku acidózy, možno tu zaradiť aj pacientov s výrazným zrakovým postihom či motorickým znevýhodnením, ktoré im neumožňujú bezpečne využiť technické aspekty pumpy a osoba je viac odkázaná na školenú asistenciu. Aj v prítomnosti kontraindikácií liečby CSII musí byť pomer benefit-riziko liečby individualizovaný [8].
Typy inzulínových púmp
V tab. 2 uvádzame najčastejšie využívané typy IP u dospelých pacientov. Výber pumpy podľa jej charakteristík je vhodné odvodiť od dominantného problému, ktorý chceme použitím CSII ovplyvniť, či sa jedná o pacientov s labilným diabetom, s častými hypoglykémiami, so syndrómom „neuvedomenia si hypoglykémie“, ktorí by profitovali z funkcie zastavenia podávania inzulínu pri hroziacej hypoglykémii (Predictive Low Glucose Suspend – PLGS), čo ale vyžaduje kontinuálny monitoring glykémie (CGM), alebo pacientov s potrebou nízkych dávok inzulínu a motorickým hendikepom pri plnení rezervoára, ktorí by profitovali z predplneného menšieho zásobníka, či pri preferencii nízkej hmotnosti zariadenia. Dôležitým parametrom výberu je aj zrakový komfort pri čítaní dát z displeja pumpy, či bezpečná obsluha funkčných tlačidiel alebo dotykového displeja.
![Stručný prehľad technických charakteristík najčastejšie používaných inzulínových púmp na
Slovensku. Upravené podľa [9,10]](https://www.forumdiabetologicum.sk/media/cache/resolve/media_object_image_small/media/image_pdf/b10665ebaf024391c7df93e58da3e74d.png)
Inzulín a CSII
Na používanie v IP sú preferované rýchloúčinkujúce inzulínové analógy, ktoré vedú k miernemu, ale signifikantnému zlepšeniu hladiny GHbA1, k lepšej dlhodobej glykemickej kontrole s nižším rizikom hypoglykémie oproti regular ľudskému inzulínu. Medzi frekventovane používané analógy patrí inzulín aspart a lispro. Efektivita týchto inzulínov z hľadiska upchatia kanyly, či komplikácií na strane infúzneho setu bola podobná, rovnako ako priemerná glykémia nimi dosiahnutá. Incidencia oklúzie je ovplyvnená opotrebovaním katétra, ale aj špecifikami jednotlivých analógov. Pri všetkých3 typoch analógov aspart, lispro a glulizín použitých v IP bola oklúzia raritná a nezávislá od výberu inzulínu počas prvých 72 hodín. Po tomto čase sa incidencia oklúzie čiastočne zvýšila, hlavne u glulizínu [4]. V prospech skoršej výmeny kanyly svedčia výsledky štúdie u pacientov s DM1T [11], ktoré potvrdili zvyšovanie glykémie už po 48 hodinách od zavedenia linky. Doba s priemernou glykémiou > 10 mmol/l sa po dobu sledovania (do 100 hodín od zavedenia kanyly) zvýšila zo 14,5 % na 38,3 %, priemerná glykémia vzrástla zo 6,8 mmol/l na 9,1 mmol/l a denná spotreba inzulínu sa zvýšila priemerne zo 48,5 IU na 55,3 IU. Odporúčania na výmenu kanyly každých 48 hodín však nie sú kompatibilné s aktuálne platnými indikačnými obmedzeniami pre preskripciu infúznych setov (podskupina D10.2.1), ktoré umožňujú predpis maximálne 10 ks/mesiac. Akceptovanie frekventnejšej výmeny kanyly by však mohlo okrem zlepšenia glykemickej kompenzácie prispieť aj k individuálne variabilnej úspore spotreby inzulínu a k zníženiu lokálnych zápalových komplikácií.
Intenzifikovaný režim, MDI v zrovnaní s CSII
Prelomové výsledky v pohľade na dopad hyperglykémií priniesla štúdia DCCT (Diabetes Control and Complications Trial) [12], ktorá jednoznačne preukázala, že striktná kontrola glykémie môže viesť k spomaleniu alebo oddialeniu progresie mikrovaskulárnych komplikácií u pacientov s DM1T. Pacienti liečení intenzívnou liečbou mali o 76 % zredukovaný vývoj diabetickej retinopatie, o 60 % diabetickej nefropatie a o 54 % diabetickej nefropatie v porovnaní s pacientami na konvenčnej liečbe. Výskum pokračoval ďalej, v nasledujúcej observačnej štúdii EDIC (Epidemiology of Diabetes and its Complications) [13] sa preukázal dlhodobý dopad striktnej liečby na udržiavanie GHbA1 približne 7,0 % na MDI/CSII oproti 9,0 % na konvenčnej liečbe. Tzv. efekt „metabolickej pamäti“ pokračoval v dopade na vznik mikrovaskulárnych komplikácií aj 4 roky po ukončení štúdie DCCT. Napriek faktu, že hladiny GHbA1 zotrvali na hodnote približne 8,0 % pre obe skupiny po ukončení DCCT, riziko redukcie nonfatálneho infarktu myokardu, mozgovej príhody alebo smrti boli redukované o 57 % 11 rokov po ukončení štúdie. Išlo o prvú štúdiu potvrdzujúcu zníženie výskytu makrovaskulárnych komplikácií v závislosti na glykemickej kontrole, no zároveň bol vyzdvihnutý benefit dôslednej glykemickej kontroly v skorých etapách ochorenia [1]. Početné systematické prehľadové články a metaanalýzy uvádzajú, že liečba CSII je v efektívnejšia v znížení GHbA1 ako MDI [1,14].
Pri porovnávaní režimu MDI s CSII v metaanalýze štúdií sa preukázalo, že priemerný rozdiel glykémií medzi skupinami bol 0,88 mmol/l (95% CI 0,5–1,2) a odlišnosť v GHbA1 0,5 % (95% CI 0,2–0,7) favorizujúc CSII. Mierna, ale signifikantne lepšia kontrola u pacientov na CSII bola spojená so 14% redukciou celkovej dennej dávky inzulínu [15]. CSII pri vysokom vstupnom GHbA1 bola efektívnejšia pri jeho redukcii ako MDI, pri hodnote vstupného GHbA1 10,0 % sa pri liečbe CSII znížil o 0,65 % oproti MDI, nenašiel sa klinicky významný rozdiel medzi skupinami v hodnote GHbA1 pokiaľ bola iniciálna hodnota GHbA1 6,5 %, taktiež sa nenašli odlišnosti v počte hypoglykemických príhod v oboch skupinách [16]. Významnosť odlišností medzi MDI a CSII vo výslednom GHbA1 v prospech CSII v selektovaných randomizovaných klinických štúdiách je uvedená v grafe 2.
![Metaanalýza efektu CSII vs. MDI na GHbA1c u detských a dospelých pacientov s DM1T.
Upravené podľa [14]](https://pl-master.mdcdn.cz/media/image_pdf/0cab235b1d2e36f6c71d225854977170.png?version=1566996091)
Intenzifikovaný inzulínový režim je vo všeobecnosti spojený s vyšším rizikom vzniku hypoglykémie, ako ukázali výsledky DCCT, podľa niektorých štúdií však CSII môže výskyt závažnej hypoglykémie redukovať v porovnaní s MDI [17–21], podľa iných jednoznačná superiorita nad MDI režimom nebola preukázaná [4,22–24]. Ukazuje sa, že riziko hypoglykémie je podobné pre obe skupiny, MDI aj CSII. Rýchlosť vzniku diabetickej ketacidózy (DKA) však môže byť vyššia u CSII oproti MDI, čo sa dá zdôvodniť tým, že CSII predstavuje viac fyziologický spôsob aplikácie inzulínu, ktorý nevytvára depozitá v podkoží, ako je tomu v MDI-režime. V prípade blokovania podávania inzulínu sa následky prejavia skôr u CSII, hlavne v ére krátkoúčinkujúcich inzulínových analógov. Inými slovami, príležitostné dlhšie prerušenie dodávky inzulínového analógu môže vyústiť do rýchlejšieho vzniku DKA. Na základe týchto poznatkov bolo odporučené, aby si pacienti užívajúci inzulínové analógy v pumpe kontrolovali ketonúriu, ev. ketonémiu pri hladovaní a pri každej príležitostnej nevysvetliteľnej vysokej glykémii > 14,0 mmol/l [8].
Literárne prehľady zaoberajúce sa nežiaducimi udalosťami pri liečbe CSII však treba posudzovať aj s ohľadom na datovanie výsledkov štúdií za posledných 30 rokov [8,25–27], kedy systém IP nebol tak prepracovaný ako dnes. Závery štúdií u detí a mladých dospelých z posledných rokov preukázali, že riziko vzniku DKA pri liečbe CSII bolo nižšie ako u MDI [17,21,28]. Rozdiely medzi MDI a CSII s použitím analógov hodnotila aj analýza, kde liečba CSII bola asociovaná s lepšou glykemickou kontrolou, bez zvýšeného rizika hypoglykémie a DKA sa vyskytovala rovnako v oboch skupinách. Porovnaním s režimom bazál-bolus má CSII superioritu, špeciálne v pediatrickej populácii [8].
Liečba CSII oproti MDI tiež preukázala lepší efekt na glykemickú variabilitu u pacientov s DM1T vo viacerých štúdiách [29,30], čo nie je zanedbateľné z hľadiska ovplyvnenia oxidačného stresu a endotelovej dysfunkcie, ktoré podľa výsledkov experimentov boli horšie pri osciláciách glykémií medzi 5,0–15,0 mmol/l každých 6 hodín počas 24 hod ako pri konštantne zvýšenej glykémii 10,0 alebo 15,0 mmo/l [31].
Zlepšenie glykemickej variability, redukcia výskytu závažnej hypoglykémie, či skrátenie času hyperglykémie významne ovplyvňuje o. i. aj rytmickú stabilitu myokardu a stabilitu aterosklerotického plátu. Prvá veľká observačná štúdia u pacientov s DM1T, ktorá sledovala vplyv inzulínovej liečby (CSII vs MDI režim) na kardiovaskulárne ochorenia a mortalitu prebehla vo Švédsku a zahŕňala takmer 20 tisíc jedincov. Pacienti s DM1T liečení CSII mali nižšiu kardiovaskulárnu mortalitu oproti pacientom, ktorí boli liečení MDI režimom [32].
Ciele nedosiahnuté – môže za to pumpa?
V manažmente liečby inzulínovou pumpou je dôležitá neustála spolupráca, ktorá si vyžaduje hlavne angažovanosť pacienta s ochotou prispôsobovať sa meniacemu sa klinickému stavu, vonkajším podmienkam alebo jednoducho starnutiu. Na druhej strane je záujem a schopnosť lekára pracovať s nastaveniami pumpy, určením timingu dávkovania inzulínu a pod. Nie je zriedkavosťou, že nedostatočná kompenzácia pacienta na inzulínovej pumpe zlyháva na banálnom podklade, ako je napr. aplikácia kanyly do lipodystrofických alebo zjazvených miest. Sú prípady, v ktorých postačí aj zmena typu kanyly, napr. zo šikmej na kolmú a pod. Samozrejmosťou je pri každej kontrole dôležité prízvukovať výmenu kanyly najneskôr na 3. deň od inzercie s pravidelnou rotáciou miesta vpichu. Všeobecne sa udáva, že medzidenná individuálna variabilita v absorpcii inzulínu je približne 25 % a variabilita medzi pacientami môže byť vyššia > 50 %. Subkutánny inzulín sa najrýchlejšie vstrebáva z podkožia brucha, nasledujú ramená, zadok a stehná, čo je závislé od regionálneho krvného prietoku. Rotácia aplikácie inzulínu je dôležitá pre vyhnutie sa vývoju lipohypertrofie alebo atrofie. Potrebné je si uvedomiť, že fyzické cvičenie zvyšuje rýchlosť absorpcie inzulínu zvýšeným prekrvením [1].
Príčinným faktorom môže byť aj nesúrodosť medzi časom podávania bolusu pred jedlom a časom samotného jedla. Tzv. čas oneskorenia, či omeškania „lag time“, je potrebné zohľadniť pri koordinácii efektu inzulínu s glykemickými exkurziami po jedle a mala by sa mu venovať pozornosť ešte pred nastavením na liečbu pumpou. Inzulínové krátkoúčinkujúce analógy by mali byť podávané 10–20 min pred jedlom, v prípade hladiny glykémie nad cieľovým rozmedzím aj 20–30 min pred jedlom v závislosti od stupňa hyperglykémie. Častejším využitím SMG alebo CGM možno upresniť vhodný čas podania inzulínu v závislosti od jedla. Použitie pre-bolusu sa ukazuje efektívne v redukcii postprandiálnych glykémií do hodnoty približne 2,8 mmol/l [1]. Samozrejmosťou je pružná korekcia bazálnych rýchlostí inzulínu po vylúčení iných príčin dysglykémie (vplyv liekov, fyzickej aktivity, nepomeru medzi bolusom a jedlom, sumácia bolusu s aktívnym inzulínom a pod).
Zvládnutie počítania sacharidových jednotiek by malo byť samozrejmosťou nielen v prípade liečby CSII, ale aj v manažmente DM všeobecne. Technológia dávkovania bazálnych dávok sa síce zdokonaľuje, ale presnosť bolusových dávok stále závisí od správneho zhodnotenia množstva sacharidov v strave. Ide o praktický návyk, ktorým pacient zhodnocuje funkciu tzv. bolusových poradcov (Bolus Wizard calculator) pri odporúčaní adekvátnej prandiálnej dávky inzulínu. Odhad množstva sacharidov v strave ostane, aspoň v najbližších rokoch, kľúčovým príspevkom pacienta k prevádzke aj ďalších generácií IP, ako je napr. Minimed 670G. Dávku bolusu tu nemožno zadať priamo ako pri bežne používaných IP, pri tomto automatickom režime sa bolus dávkuje len na základe zadaného množstva sacharidov.
Záver
Závery štúdií DCCT a EDIC jednoznačne preukázali dlhodobý benefit striktnej glykemickej kontroly DM1T vo včasných štádiách na vývoj mikrovaskulárnych a aj makrovaskulárnych komplikácií. Použitie CSII u DM1T je viac efektívne v dosiahnutí redukcie GHbA1 a glykemickej variability ako MDI, bez signifikantných odlišností vo vzniku závažnej hypoglykémie.
Výberom a iniciálnym nastavením pacienta na liečbu CSII však problém liečby diabetu nie je zďaleka vyriešený, inzulínová pumpa je len prostriedkom k dosiahnutiu adekvátnych výsledkov, nie terapeutickým stropom. Na strane pacienta liečeného CSII ostáva dôležitá adherencia k liečbe, ochota spolupráce, sebakontroly, na strane lekára je ťarcha problémov v identifikovaní problematických oblastí, ale aj umenie ich pružne ovplyvňovať a normalizovať. Bez týchto osobných vkladov sa aj sofistikovaný nástroj liečby diabetu, akým je inzulínová pumpa, stáva len drahým technickým „doplnkom“.
MUDr. Dana Prídavková, PhD.
Doručené do redakcie 23. 3. 2019
Prijaté po recenzii 26. 4. 2019
Sources
- Subramanian S, Baidal D, Skyler JS et al. The Management of Type 1 Diabetes [Updated 2017]. In: Feingold KR, Anawalt B, Boyce A et al. Endotext, South Darthmouth (MA): MDText.com, Inc., 2000. Dostupné z WWW: <https://www.ncbi.nlm.nih.gov/pubmed/25905160>.
- Kesavadev J, Kumar Das A, Unnikrishnan R et al. Use of Insulin Pumps in India: Suggeseted Guidelines Based on Experience and Cultural Difference. Diabetes Technol Ther 2010; 12(10): 823–831. Dostupné z DOI: <http://dx.doi.org/10.1089/dia.2010.0027>.
- Pickup JC, Keen H, Parsons JA et al. Continuous subcutaneous insulin infusion: an approach to achieving normoglycaemia. Br Med 1978; 1(6107): 204–207.
- Pozzilli P, Battelino T, Danne T et al. Continuous subcutaneous insulin infusion in diabetes: patient populations, safety, efficacy, and pharmacoeconomics. Diabetes Metab Res Rev 2016; 32(1): 21–39. Dostupné z DOI: <http://dx.doi.org/10.1002/dmrr.2653>.
- Doničová V, Brož J, Sorin I. Health Care Provision for People with Diabetes and Postgraduate Training of Diabetes Specialists in Eastern European Countries. J Diabetes Sci Technol 2011; 5(5): 1124–1136. Dostupné z DOI: <http://dx.doi.org/10.1177/193229681100500513>.
- Renard E. Insulin pump use in Europe. Diabetes Technol Ther 2010; 12(Suppl1): S29-S32. Dostupné z DOI: <http://dx.doi.org/10.1089/dia.2009.0189>.
- Martinka E, Mokáň M, Uličiansky V et al. Konsenzuálny terapeutický algoritmus pre liečbu pomocou inzulínovej pumpy a kontinuálne meranie glykémie (v súlade s aktuálnym znením indikačných obmedzení). Forum Diab 2016; 5(2): 111–120.
- Hannaire H, Lassmann-Vague V, Jeandidier N et al. Treatment of diabetes mellitus using an external insulin pump: the state of the art. Diabetes and metabolism 2008; 34(4 Pt 2): 401–423. Dostupné z DOI: <http://dx.doi.org/10.1016/S1262–3636(08)73972–7>.
- Reznik Y (ed). Handbook of Diabetes Technology. Springer International 2019. Hardcover ISBN 978–3-319–98118–5. eBook ISBN 978–3-319–98119–2. Dostupné z DOI: <http://dx.doi.org/10.1007/978–3-319–98119–2>.
- User Manual for Dana Diabecare R. Dostupné z WWW: <http://www.sooil.com/bbs/board.php?bo_table=data_eng&wr_id=11&sca=Manuals>.
- Thethi TK, Rao A, Kawji H et al. Consequences of delayed pump infusion line change in patients with Type 1 diabetes mellitus treated with continuous subcutaneous insulin infusion. J Diabetes Complications 2010; 24(2): 73–78. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jdiacomp.2009.03.002>
- Nathan DM, Genuth S, Lachin J et al. [Diabetes Control and Complications Trial Research Group]. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med 1993; 329(14): 977–986. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJM199309303291401>.
- Nathan DM, Cleary PA, Backlund JY et al. Intensive diabetes treatment and cardiovascular disease in patients with type 1 diabetes. N Engl J Med 2005; 353(25): 2643–2653. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa052187>.
- Misso ML, Egberts KJ, Page M et al. Continuous subcutaneous insulin infusion (CSII) versus multiple daily injections for type 1 diabetes mellitus. Cochrane Database Syst Rev 2010; (1):CD005103. <http://dx.doi.org/10.1002/14651858.CD005103.pub2>.
- Hirsch IB, Bode BW, Garg S et al. Continuous subcutaneous insulin infusion (CSII) of insulin aspart versus multiple daily injections of insulin aspart/insulin glargin in type 1 diabetic patients previously treated with CSII. Diabetes Care 2005; 28(3):533–538.
- Retnakaran R, Hochman J, DeVries JH et al. Continuous subcutaneous insulin infusion versus mlutiple daily injections: The impact of baseline A1c. Diabetes Care 2004; 27(11): 2590–2596.
- Karges B, Schwandt A, Heidtmann B et al. Association of insulin pump therapy vs insulin injection therapy with severe hypoglycemia, ketoacidosis, and glycemic control among children, adolescents, and young adults with type 1 diabetes. JAMA 2017; 318(14): 1358–1366. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2017.13994>.
- Haynes A, Hermann JM, Miller KM et al. Severe hypoglycemia rates are not associated with HbA1c: a cross-sectional analysis of 3 contemporary pediatric diabetes registry databases. Pediatr Diabetes 2017; 18(7): 643–650. Dostupné z DOI: <http://dx.doi.org/10.1111/pedi.12477>.
- Pickup JC, Sutton AJ. Severe hypoglycaemia and glycaemic control in type 1 diabetes: metaanalysis of multiple daily insulin injections compared with continuous subcutaneous insulin infusion. Diabet Med 2008; 25(7): 765–774. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1464–5491.2008.02486.x>.
- Birkebaek NH, Drivvoll AK, Aakeson K et al. Incidence of severe hypoglycemia in children with type 1 diabetes in the Nordic countries in the period 2008–2012: association with hemoglobin A1c and treatment modality. BMJ Open Diabetes Res Care 2017; 5(1): e000377. Dostupné z DOI: <http://dx.doi.org/10.1136/bmjdrc-2016–000377>.
- [American Diabetes Association] Standards of Medical Care in Diabetes -2019. Diabetes Care 2019; 42(Suppl 1): S1-S2. Dostupné z DOI: < https://doi.org/10.2337/dc19-Sint01>.
- [Medical Advisory Secretariat]. Continuous subcutaneous insulin infusion pumps for type 1 and type 2 adult diabetic populations: an evidence‐based analysis. Ontario Health Technology Assessment 2009; 9(20): 1–58.
- Jeitler K, Horvath K, Berghold A et al. Continuous subcutaneous insulin infusion versus multiple daily insulin injections in patients with diabetes mellitus: systematic review and meta‐analysis. Diabetologia 2008;51(6): 941–951. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–008–0974–3>.
- Jacobsen IB, Henriksen JE, Hother‐Nielsen O et al. Evidence‐based insulin treatment in type 1 diabetes mellitus. Diabetes Res Clin Pract 2009; 86(1): 1–10. Dostupné z DOI: <http://dx.doi.org/10.1016/j.diabres.2009.05.020>.
- Chantelau E, Spraul M, Mühlhauser I et a. Long-term safety, efficacy and side-effects of continuous subcutaneous insulin infusion treatment for type 1 (insulin-dependent) diabetes mellitus: a one centre experience. Diabetologia 1989; 32(7): 421–426.
- [Diabetes Control and Complications Trial Research Group]. Adverse events and their association with treatment regimens in the diabetes control and complications trial. Diabetes Care 1995;18(11): 1415–1427.
- Egger M, Davey Smith G, Stettler C et al. Risk of adverse effects of intensified treatment in insulin-dependent diabetes mellitus: a meta-analysis. Diabet Med 1997; 14(11): 919–928. Dostupné z DOI: <http://dx.doi.org/10.1002/(SICI)1096–9136(199711)14:11<919::AID-DIA456>3.0.CO;2-A>.
- Maahs DM, Hermann JM, Holman N et al. [National Paediatric Diabetes Audit and the Royal College of Paediatrics and Child Health, the DPV Initiative, and the T1D Exchange Clinic Network]. Rates of diabetic ketoacidosis: international comparison with 49,859 pediatric patients with type 1 diabetes from England, Wales, the U.S., Austria, and Germany. Diabetes Care 2015; 38(10): 1876–1882. Dostupné z DOI: <http://dx.doi.org/10.2337/dc15–0780>.
- Maiorino MI, Bellastella G, Casciano O et al. The Effects of Subcutaneous Insulin Infusion Versus Multiple Insulin Injections on Glucose Variability in Young Adults with Type 1 Diabetes: The 2-Year Follow-Up of the Observational METRO Study. Diabetes Technol Ther 2018; 20(2): 117–126. Dostupné z DOI: <http://dx.doi.org/10.1089/dia.2017.0334>.
- Leporo G, Corsi A, Dodesini AR et al. Continuous Subcutaneous Insulin Infusion Is Better Than Multiple Daily Insulin Injections in Reducing Glucose Variability Only in Type 1 Diabetes With Good Metabolic Control. Diabetes Care 2010; 33(6): e81-e81. Dostupné z DOI: <https://doi.org/10.2337/dc10–0355>.
- Ceriello A, Esposito K, Piconi L et al. Oscillating glucose is more deleterious to endothelial function and oxidative stress than mean glucose in normal and type 2 diabetic patients. Diabetes. 2008; 57(5): 1349–1354. Dostupné z DOI: <http://dx.doi.org/10.2337/db08–0063>.
- Steineck I, Cederholm J, Eliasson B et al. Insulin pump therapy, multiple daily injections, and cardiovascular mortality in 18 168 people with type 1 diabetes: observational study. BMJ 2015; 350:h3234. Dostupné z DOI: <http://dx.doi.org/10.1136/bmj.h3234>.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Forum Diabetologicum

2019 Issue 2
Most read in this issue
- Moderné trendy v liečbe hypertenzie
- Novinky vo farmakoterapii obezity
- Moderné trendy v lokálnej liečbe diabetickej nohy
- Liečba diabetes mellitus 1. typu pomocou inzulínovej pumpy – komu a prečo?
