Kde sme a kam smerujeme v prevencii aterosklerózy u pacientov s diabetom 2. typu?
Where are we and where are we headed in the prevention of atherosclerosis in patients with type 2 diabetes
Complications of atherosclerosis, namely coronary heart disease, cerebrovascular ischemia and peripheral artery disease, are a major cause of morbidity and mortality in patients with type 2 diabetes. Significant success have been achieved in atherosclerosis prevention in diabetes with multifactorial interventions targeting risk factors for atherosclerosis. Multifactorial interventions have halved the risk of developing cardiovascular events. Additional contributions in reducing cardiovascular mortality have been made by antidiabetic agents that have additive effects on atherosclerosis progression or treatment of heart failure, such as GLP-1 receptor agonists and SGLT2 inhibitors, respectively. The goals that previous pharmacological interventions have failed to achieve sufficiently are bigger weight reduction and reduction of triacylglyceride levels. With respect to weight reduction, high-dose GLP-1 receptor agonists or dual GLP-1/GIP receptor agonist treatment is promising. New classes of drugs that will be able to reduce triglyceride levels more significantly are also currently under development.
Keywords:
obesity – triglycerides – Atherosclerosis – type 2 diabetes – GLP-1 receptor agonists
Autoři:
Ivan Tkáč
Působiště autorů:
Excelentný tím pre výskum aterosklerózy (EXTASY), IV. interná klinika UPJŠ LF a UN LP, Košice
Vyšlo v časopise:
Forum Diab 2023; 12(1): 46-51
Kategorie:
Prehľadové práce
Souhrn
Komplikácie aterosklerózy, hlavne koronárna choroba srdca, cerebrovaskulárna ischémia a periférne artériové obliterujúce ochorenie sú závažnou príčinou morbidity a mortality u pacientov s diabetom 2. typu. V prístupe k prevencii aterosklerózy pri diabete sa dosiahli významné úspechy multifaktoriálnymi intervenciami zameranými na rizikové faktory aterosklerózy, ktorými sa podarilo znížiť riziko rozvoja kardiovaskulárnych (KV) príhod na polovicu. O ďalší prínos v znížení KV-mortality sa zaslúžili antidiabetiká, ktoré majú prídavné účinky na progresiu aterosklerózy, ako sú preparáty zo skupiny agonistov GLP1-receptorov, prípadne liečbu na srdcového zlyhávania, ako sú inhibítory SGLT2. Ciele, ktoré sa predchádzajúcimi farmakologickými intervenciami nepodarilo dosiahnuť v dostatočnej miere, sú výraznejšia redukcia hmotnosti a zníženie hladín triacylglycerolov. V redukcii hmotnosti sú perspektívne vysoké dávky agonistov GLP1-receptorov alebo duálnych agonistov GLP1 a GIP-receptorov. V súčasnosti sú vo vývoji aj nové skupiny liekov, ktoré budú schopné znížiť výraznejšie hladinu triacylglycerolov.
Klíčová slova:
ateroskleróza – obezita – diabetes mellitus 2. typu – agonisty GLP1-receptorov – triacylglyceroly
Úvod
Komplikácie aterosklerózy, hlavne koronárna choroba srdca, cerebrovaskulárna ischémia a periférne artériové obliterujúce ochorenie sú závažnou príčinou morbidity, mortality a invalidity u pacientov s ochorením diabetes mellitus 2. typu (DM2T). Namiesto v minulosti preferovaného termínu makrovaskulárne komplikácie diabetu sa v súčasnosti častejšie používa vhodnejší termín kardiovaskulárne ochorenia (KVO) asociované s diabetom z nasledovných dôvodov: KVO sa často manifestujú už v období pred diagnózou DM2T ako následok metabolického syndrómu. Prítomnosť DM2T vedie k ich zvýšenej incidencii ako aj akcelerácii progresie, takže v konečnom dôsledku je výskyt KVO pri DM2T 2- až 3-násobne vyšší ako u rovnako starej populácie bez diabetu a ďalej sa zvyšuje v závislosti od trvania DM2T [1].
Ovplyvnenie rozvoja KVO pri DM2T sa dlho sústreďovalo na ovplyvnenie jednotlivých rizikových faktorov aterosklerózy. Z nich bolo najefektívnejšie zníženie LDL-cholesterolu (LDL-C) a krvného tlaku. Metaanalýza štúdií so statínmi ukázala, že zníženie hladiny LDL-C o 1 mmol/l vedie pri DM2T k zníženiu celkovej mortality o 9 %, kardiovaskulárnej (KV) mortality o 13 %, závažných koronárnych príhod o 23 % a cievnych mozgových príhod (CMP) o 17 % [2]. Podobne aj metaanalýza štúdií antihypertenzívnej liečby pri DM2T ukázala, že zníženie systolického tlaku krvi o 10 mmHg viedlo k zníženiu celkovej mortality o 13 %, CHD o 12 % a CMP o 27 % [3].
Menej jednoznačný bol vzťah zníženia glykémie (HbA1c) k prevencii KVO pri použití klasických antidiabetík (metformín, deriváty sulfonylurey, inzulín, glitazóny). Metaanalýza 4 veľkých štúdií zameraných na dosiahnutie čo najnižších hladín HbA1c v intenzívne liečenej skupine ukázala, že zníženie HbA1c o 1 % viedlo k signifikantnej redukcii incidencie infarktu myokardu (IM) o 15 %, zatiaľ čo nemalo prakticky žiadny efekt na incidenciu CMP, KV- a celkovú mortalitu [4].
Klinika Steno Diabetes Center v Kodani vykonala štúdiu intervencií na všetky ovplyvniteľné rizikové faktory aterosklerózy známu pod názvom Steno-2. Do štúdie boli zaradení pacienti s diabetom 2. typu a mikroalbuminúriou. V intenzívne liečenej skupine boli intervencie zamerané na agresívne ovplyvnenie glykemickej kompenzácie, krvného tlaku, dyslipidémie, režimové opatrenia, ako aj antiagregačnú liečbu kyselinou acetylsalicylovou. Štúdia trvala v priemere 7,8 roku. Jej výsledky boli publikované v roku 2003, keď v skupine pacientov s intenzívnymi intervenciami bolo pozorované signifikantné zníženie incidencie KVO o 53 %. Zaujímavým faktom je, že „efekt dedičstva“ (legacy effect) pretrvával ešte aj po 21 rokoch, teda 13 rokov po ukončení štúdie. Celková mortalita po tomto období bola signifikantne znížená o 45 % a KV-mortalita až o 62 %. Tento rozdiel sa premietol do predĺženia života v mediáne o 8 rokov [5]. Multifaktoriálne intervencie boli teda efektívnym prístupom k liečbe, ale stále ostával významný podiel pacientov s DM2T, u ktorých nemali dostatočný efekt. Preto sa vystupňovalo úsilie zamerané na ďalšie zníženie incidencie KVO a s nimi združenej mortality.
Nové prístupy k liečbe diabetu a obezity
Po roku 2005 sa uviedli do liečby 3 nové skupiny antidiabetík, ktorých mechanizmus účinku sa odlišoval od predchádzajúcich antidiabetík používaných v klinickej praxi. Dve skupiny liekov patrili do skupiny inkretínových mimetík, ktoré napodobňujú účinky gastrointestinálnych hormónov glukagónu podobného peptidu 1 (GLP1) a glukózo-dependentného inzulínotropného peptidu (GIP), a to perorálne inhibítory DPP4 (DPP4i) a subkutánne podávané agonisty receptorov pre GLP1 (GLP1-RA). Pri zavedení týchto liekov do praxe sa ich najväčšou výhodou voči sulfonylureovým sekretagogám a inzulínom javila absencia hypoglykémií pri liečbe, nakoľko stimulácia sekrécie inzulínu inkretínovými mimetikami je glukózodependentná, teda sa „vypína“ pri dosiahnutí normálnych hodnôt glykémie. Navyše GLP1-RA mali aj signifikantný efekt na zníženie telesnej hmotnosti na rozdiel od sulfonylurey, glitazónov a inzulínu, ktoré všetky vedú k zvyšovaniu telesnej hmotnosti [6]. Navyše liečba glitazónmi viedla aj k zvýšenej incidencii srdcového zlyhávania a pri metaanalýze štúdií s rosiglitazonom bolo referované aj zvýšenie incidencie infarktu myokardu (IM) [7]. Ďalšou skupinou novo zavedených antidiabetík boli inhibítory sodíkovo glukózového kotransportéra 2 (SGLT2i), ktorý svojím účinkom v proximálnych tubuloch obličiek zvyšujú glukozúriu a nátriúriu [8].
Do roku 2015 tak jediným antidiabetikom s dokázaným preventívnym účinkom voči rozvoju aterosklerózy bol metformín, ktorého priaznivé účinky v prevencii IM a celkovej mortality boli popísané už v štúdii UKPDS, ktorá bola publikovaná v roku 1998 [9].
Na základe podozrenia na proaterogénny účinok rosiglitazonu a preukázaného proaterogénneho účinku muraglitazaru – duálneho agonistu peroxizómovým proliferátorom aktivovaných receptorov (PPAR)α/δ, sa v roku 2008 rozhodli regulačné úrady Food and Drug Administration USA (FDA) a European Medicines Agency EÚ (EMA) požadovať u nových antidiabetík zavedených do klinickej praxe postregistračné štúdie KV-bezpečnosti [7]. Viaceré tieto štúdie nielenže dokázali KV-bezpečnosť nových antidiabetík, ale aj ich priaznivý efekt na zníženie incidencie KV-príhod.
Prvou takouto štúdiou, bola v roku 2015 publikovaná štúdia s SGLT2i empagliflozínom (EMPA-REG OUTCOME). Prídavná liečba empagliflozínom k predchádzajúcej antidiabetickej liečbe v porovnaní s placebom signifikantne znížila incidenciu primárneho kompozitného výsledku pozostávajúceho z KV-mortality, nefatálneho IM alebo nefatálnej CMP o 12 %. Kým v tejto štúdii nebol pozorovaný efekt na incidenciu IM alebo CMP, KV-mortalita bola signifikantne redukovaná o 36 % a celková mortalita o 32 %. Tento nesúlad v efekte na súčasti primárneho výsledku vysvetľoval sekundárny ukazovateľ hospitalizácia pre srdcové zlyhávanie (HSZ), ktorej incidencia bola pri liečbe empagliflozínom signifikantne znížená o 36 % [10]. Ďalšie štúdie KV-bezpečnosti s kanagliflozínom, dapagliflozínom a ertugliflozínom v zásade potvrdili skupinový efekt inhibície SGLT2, i keď veľkosť efektu na jednotlivé výsledky sa líšila, ale metaanalýza nezistila signifikantnú heterogenitu medzi efektom jednotlivých preparátov. Vo všetkých štyroch štúdiách bol efekt jednotlivých SGLT2i na redukciu HSZ štatisticky významný [11].
V nasledujúcom roku po publikovaní výsledkov EMPA-REG OUTCOME boli publikované výsledky štúdie KV-bezpečnosti s GLP1-RA liraglutidom (LEADER). Aj v tejto štúdii bolo zistené signifikantné zníženie primárneho kompozitného výsledku (KV-mortalita, nefatálny IM alebo nefatálna CMP) pri prídavnej liečbe liraglutidom v porovnaní s placebom o 13 %. Taktiež bola pozorovaná signifikantná redukcia KV-mortality o 22 %, celkovej mortality o 15 % a fatálneho alebo nefatálneho IM o 14 % [12]. V tom istom roku boli publikované výsledky ďalšej štúdie s GLP1-RA semaglutidom (SUSTAIN-6). V tejto štúdii viedla liečba semaglutidom k signifikantnej redukcii primárneho kompozitného výsledku o 26 % a incidencie CMP o 39 % [13]. Z ďalších šiestich štúdií KV-bezpečnosti s GLP1-RA bolo zistené signifikantné zníženie incidencie primárneho kompozitného výsledku v štúdiách s albiglutidom, dulaglutidom a efpeglenatidom, zatiaľ čo v štúdiách s exenatidom a perorálnym semaglutidom síce nebola zistená signifikantná redukcia primárneho výsledku, ale bolo pozorované signifikantné zníženie dôležitého sekundárneho výsledku – celkovej mortality [14].
Metaanalýzy primárnych a vybraných sekundárnych KV-výsledkov v štúdiách s SGLT2i a GLP1-RA sú uvedené v tab. 1. Ak porovnáme výsledky metaanalýz v tab. 1, je zrejmé, že SGLT2i a GLP1-RA majú prakticky rovnaký efekt na primárny kompozitný ukazovateľ, KV-mortalitu a celkovú mortalitu. Efekt SGLT2i na incidenciu IM a CMP nebol signifikantný, ale majú výrazný efekt na zníženie incidencie HSZ. Na druhej strane, GLP1-RA znižujú štatisticky významne incidenciu IM a ešte výraznejšie CMP. Navyše metaanalýza uvedených štúdií s ukázala, že liečba SGLT2i bola asociovaná so signifikantným zvýšením amputácií dolných končatín o 25 % [11], zatiaľ čo v štúdiách s GLP1-RA bola incidencia amputácií dolných končatín sledovaná iba v štúdii s liraglutidom, v ktorej bol pozorované signifikantné zníženie incidencie amputácií o 35 % [15]. Na základe formálneho porovnania efektu na jednotlivé KV-výsledky je pravdepodobné, že SGLT2i znižujú mortalitu prostredníctvom ich účinku na srdcové zlyhávanie [16] a spomalenie progresie chronickej obličkovej choroby [11], zatiaľ čo konzistentný efekt GLP1-RA na všetky zložky primárneho výsledku naznačuje ich antiaterogénny efekt [14].
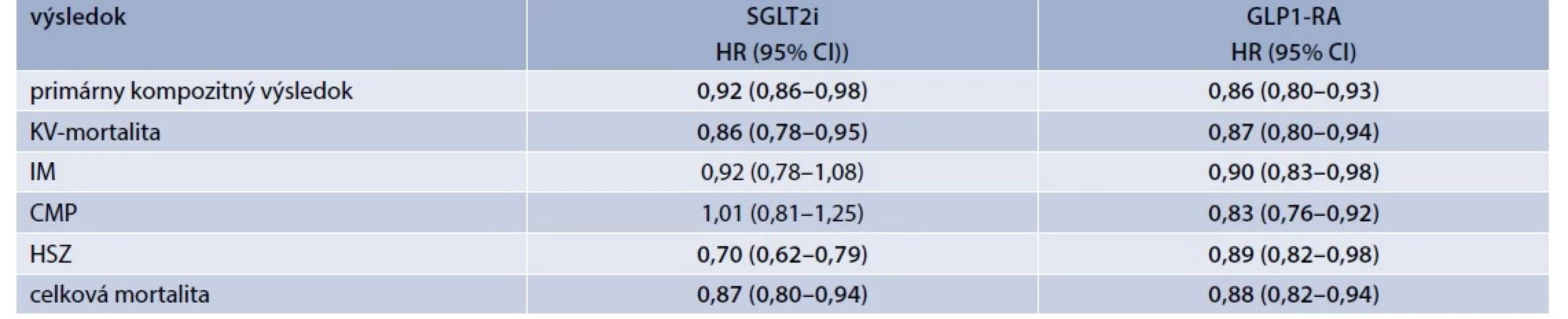
Poznámka: HR zvýraznené tučným písmom indikujú signifikantné zníženie pravdepodobnosti výsledku pri liečbe uvedenou skupinou liekov.
Mechanizmus účinku agonistov GLP1-receptorov
Antiaterogénny efekt GLP1-RA bol v posledných rokoch podrobne skúmaný, nakoľko GLP1-RA sa nachádzajú okrem pankreatických B-buniek aj v mnohých iných tkanivách, napr. v endoteli ciev, srdcovom svale, črevnej a žalúdočnej sliznici a oblastiach mozgu zahrňujúcich centrum sýtosti [6]. Mediačná analýza zo štúdie LEADER ukázala, že efekt liraglutidu na redukciu KV-výsledkov bol čiastočne sprostredkovaný jeho vplyvom na zníženie HbA1c a albuminúriu [17]. Albuminúriu možno v kontexte sprostredkovania liečebného efektu vnímať ako proxy (náhradný ukazovateľ) endotelovej dysfunkcie. Okrem toho liečba antidiabetickými dávkami GLP1-RA (napr. semaglutidom v dávke 1 mg s.c. týždenne) viedla k zníženiu telesnej hmotnosti v priemere o 4,9 kg [13]. I keď v mediačnej analýze nebolo zníženie telesnej hmotnosti asociované s priaznivým efektom na redukciu KVO, v súčasnej dobe sa testujú vyššie dávky GLP1-RA na liečbu obezity, a to aj u obéznych jedincov bez diabetu.
Na liečbu obezity bola testovaná dávka semaglutidu 2,4 mg/týždeň. U obéznych jedincov bez diabetu došlo k poklesu telesnej hmotnosti až o 15 % od východiskových hodnôt [18]. U pacientov s diabetom bol pozorovaný o niečo nižší pokles telesnej hmotnosti, a to o 10 % z bazálnych hodnôt [19].
Ďalší preparát zo skupiny inkretínových mimetík – duálny agonista GLP1 a GIP-receptorov tirzepatid – bol tiež testovaný na liečbu obezity u jedincov bez diabetu. Pri jeho maximálnej dávke 15 mg subkutánne raz týždenne bol pozorovaný pokles oproti bazálnym hladinám telesnej hmotnosti o 21 % [20]. Aj v tejto štúdii bol u pacientov s DM2T pri liečbe tirzepatidom pokles z bazálnych hladín menší ako u nediabetikov, a to o 11 % z bazálnych hodnôt [21]. To nasvedčuje, že u pacientov s DM2T je prítomná rezistencia voči stimulácii receptorov pre GLP1, podobne ako je prítomná inzulínová rezistencia. Efekt vyššie uvedených agonistov inkretínových receptorov na telesnú hmotnosť sa blíži účinku bariatrickej chirurgie, ktorá bola doteraz jedinou intervenciou voči obezite, ktorá bola asociovaná so znížením KV-morbidity a mortality [22]. Avšak iba prebiehajúce klinické randomizované štúdie ukážu, či efekt GLP1-RA a duálnych agonistov na obezitu bude mať prídavný efekt na zníženie incidencie KV-príhod, prípadne aj mortality aj u pacientov s DM2T.
Nové možnosti v liečbe hypertriacylglycerolémie
Hypertriacylglycerolémia (HTG) je súčasťou fenotypu aterogénnej (alternatívne nazývanej aj diabetickej) dyslipidémie spolu so zníženou hladinou HDL-cholesterolu (HDL-C), zvýšeným zastúpením aterogénnych malých denzných častíc LDL (mdLDL) a zvýšeným apolipoproteínom B (apoB), ktorý reflektuje počet všetkých častíc VLDL, IDL a LDL. Už pred štvrťstoročím Tkáč et al ukázali, že angiografická závažnosť koronárnej aterosklerózy u pacientov s DM2T najtesnejšie koreluje s hladinou apoB v lipoproteínoch bohatých na triacylglyceroly (TAG), teda vo VLDL a IDL [23].
I keď epidemiologické štúdie naznačovali už desaťročia rizikovosť HTG, vo vzťahu k aterogenite lipoproteínov bohatých na TAG existovali viaceré kontroverzie, keďže sa nepodarilo dokázať prítomnosť TAG v aterómových plátoch. Viacerí autori však jednoznačne dokázali, že chylomikrónové a VLDL-remnanty (zvyšky po lipolýze lipoproteínovou lipázou) sú nosičmi cholesterolu do cievnej steny [24]. Navyše, čím je vyššia hladina TAG, tým je vyššie zastúpenie mdLDL, pričom mdLDL začínajú dominovať nad väčšími, menej aterogénnymi časticami LDL približne pri hladine TAG 1,2 mmol/l. Aj nedávno publikovaný Konsenzus Európskej spoločnosti pre aterosklerózu (EAS) definuje hladinu TAG < 1,2 mmol/l ako optimálnu, i keď terapeutický cieľ pri liečbe HTG je stanovený < 1,7 mmol/l [24].
Pacienti s DM2T profitujú zo zníženia LDL cholesterolu (LDL-C) podobným znížením relatívneho rizika a väčším znížením absolútneho rizika rozvoja KV-príhod ako jedinci bez diabetu, ako ukázali aj štúdie s inhibítormi PCSK9, pri ktorých sa agresívne liečené skupiny chorých dostali až na hladiny LDL-C okolo 1 mmol/l [25,26].
Prínos zníženia TAG nebol zatiaľ jednoznačne dokázaný. Zatiaľ čo fibráty znižovali hladiny TAG najviac z dostupných hypolipidemík, prínos liečby fibrátmi u pacientov s DM2T nebol pozorovaný. V štúdii FIELD bolo testovaná liečba fenofibrátom u pacientov s DM2T, ktorí na začiatku štúdie neužívali statín. V priebehu štúdie začalo užívať aj inú hypolipidemickú liečbu 36 % pacientov v placebovej skupine a 19 % v skupine liečenej fenofibrátom. Výskyt primárneho kompozitného výsledku (mortalita na CHD alebo nefatálny IM) nebol signifikantne odlišný medzi porovnávanými skupinami [27]. V štúdii ACCORD Lipid bol fenofibrát pridávaný k predchádzajúcej liečbe simvastatínom pacientom s DM2T. Podobne ako v predchádzajúcej štúdii nebol pozorovaný signifikantný rozdiel v incidencii primárneho kompozitného výsledku (nefatálny IM, nefatálna CMP alebo KV-mortalita) medzi skupinou užívajúcou fenofibrát a placebo [28].
V oboch zmienených štúdiách bol v podskupinovej analýze naznačený lepší efekt fenofibrátu u pacientov s diabetickou dyslipidémiou (TAG > 2,3 mmol/l, HDL-C < 1,0 mmol/l) [27,28]. Na základe týchto dát bola dizajnovaná ďalšia štúdia, ktorá testovala efekt pemafibrátu na výskyt KV-príhod u pacientov s DM2T a diabetickou dyslipidémiou (PROMINENT). Do štúdie boli zaradení pacienti, ktorí užívali hypolipidemickú liečbu podľa terapeutických odporúčaní alebo nemohli užívať statíny pre ich vedľajšie účinky. Ani v tejto štúdii nebol pozorovaný signifikantný rozdiel v incidencii primárneho kompozitného výsledku (nefatálny IM, ischemická CMP, koronárna revaskularizácia alebo KV-mortalita) medzi skupinou chorých liečených pemafibrátom a placebom [29]. Na základe výsledkov uvedených 3 štúdií sa nejavia fibráty ako vhodná liečba na prevenciu KV-výsledkov u pacientov s DM2T a HTG, i keď stále sú vhodné ako prevencia rozvoja akútnej pankreatitídy u jedincov s výraznej zvýšenými hladinami TAG.
Efekt omega 3 mastných kyselín na zníženie hladiny TAG je známy už dávnejšie, ale žiadna z novších štúdií nedokázala ich priaznivý efekt na KV-príhody u pacientov, ktorí užívali statíny. Preto boli určitým prekvapením výsledky štúdie REDUCE-IT. Do tejto štúdie boli zaradení pacienti s preexistujúcim KVO alebo diabetom, ktorí mali hladiny TAG v rozmedzí 1,5–5,6 mmol/l a LDL-C v rozmedzí 1,1–2,6 mmol/l pri liečbe statínmi. Pacienti boli randomizovaní na liečbu ikozapentetylom (IPE – etyl ester kyseliny eikozapentaénovej) v dávke 4 g denne alebo na placebo. Pri liečbe IPE bolo pozorované signifikantné zníženie incidencie primárneho kompozitného výsledku (KV-mortalita, nefatálny IM alebo nefatálna CMP) o 26 %. Výsledky vo veľkej podskupine diabetikov (30 % študijnej populácie) boli identické s výsledkami v celom súbore. I keď bola štúdia primárne zacielená na jedincov s HTG, pri liečbe IPE bola pozorovaná priemerná redukcia hladiny TAG o 20 % v porovnaní s placebom, ktorá bola menšia ako priemerná redukcia TAG v štúdiách s fibrátmi [30]. Navyše, koncová dosiahnutá hladina TAG (priemer 2,0 mmol/l) bola ďaleko vyššia ako hladina 1,2 mmol/l považovaná EAS za optimálnu a dokonca aj vyššia ako 1,7 mmol/l, ktorá je momentálne považovaná za cieľovú. To naznačuje, že pravdepodobne aj iné faktory ako redukcia TAG prispeli k efektu IPA v tejto štúdii.
Lepšia glykemická kompenzácia vedie k zníženiu hladiny TAG, nakoľko menšie množstvo nadbytočnej glukózy v krvnom obehu je k dispozícii pre tvorbu triacylglycerolov. Z antidiabetík majú GLP1-RA navyše aditívny efekt na ovplyvnenie HTG, keďže blokujú tvorbu chilomikrónov v črevnej stene, a tým znižujú aj množstvo aterogénnych chilomikrónových remnantov v obehu. V štúdii s perorálnym semaglutidom bola pri dávke 14 mg denne znížená hladina TAG nalačno o 20 % a plocha pod krivkou postprandiálnej triacylglycerolémie o 32 %. Plocha pod krivkou apoB48, ktorý je súčasťou chilomikrónových remnantov, sa znížila pri užívaní semaglutidu až o 45 %, čo ukazuje, že efekt na postprandiálnu triacylglycerolémie je výraznejší ako na hladiny TAG nalačno [31].
Záverom možno konštatovať, že v prístupe k prevencii aterosklerózy pri DM2T sa dosiahli významné úspechy multifaktoriálnymi intervenciami na rizikové faktory aterosklerózy, ktorými sa podarilo znížiť riziko rozvoja KV-príhod na polovicu. O ďalší prínos sa zaslúžili antidiabetiká, ktoré majú prídavné účinky na prevenciu aterosklerózy ako preparáty zo skupiny GLP1-RA. Ďalšie dva ciele, ktoré sa predchádzajúcimi farmakologickými intervenciami nepodarilo dosiahnuť pri DM2T, sú redukcia hmotnosti o viac ako 10 % a zníženie hladín TAG na optimálne hodnoty < 1,2 mmol/l. V redukcii hmotnosti sú perspektívne vysoké dávky GLP1-RA alebo duálnych agonistov GLP1 a GIP-receptorov. V súčasnosti sú vo vývoji aj nové skupiny liekov, ktoré sú schopné znížiť hladinu TAG až o približne 60 %, ako je vupanorsen [32].
Prehlásenie o potenciálnom konflikte záujmov
Autor obdržal honoráre za prednáškovú a konzultačnú činnosť od spoločností Boehringer Ingelheim, Dôvera ZP, Eli Lilly a Novo Nordisk.
Publikácia bola podporená grantom VEGA 1/0183/20.
prof. MUDr. Ivan Tkáč, PhD.
www.upjs.sk
Doručené do redakcie | Received 25. 2. 2023
Prijaté po recenzii | Accepted 8. 3. 2023
Zdroje
1. La Sala L, Prattichizzo F, Ceriello A. The link between diabetes and atherosclerosis. Eur J Prev Cardiol 2019; 26(2 Suppl): 15–24. Dostupné z DOI: <http://dx.doi.org/10.1177/2047487319878373>.
2. Kearney PM, Blackwell M, Collins L et al. [Cholesterol Treatment Trialists (CTT) Collaboration]. Efficacy of cholesterol-lowering therapy in 18,686 people with diabetes in 14 randomised trials of statins: a meta-analysis. Lancet 2008; 371(9607): 117–125. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(08)60104-X>
3. Emdin CA, Rahimi K, Neal B et al. Bllod pressure lowering in type 2 diabetes: a systemic review and meta-analysis. JAMA 2015; 313(6): 603–615. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2014.18574>.
4. Turnbull FM, Abraira C, Anderson RJ et al. Intensive glucose control and macrovascular outcomes in type 2 diabetes. Diabetologia 2009; 52(11): 2288–2298. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–009–1470–0>.
5. Gaede P, Oellgaard J, Carstensen B et al. Years of life gained by multifactorial intervention in patients with type 2 diabetes mellitus and microalbuminuria: 21 years follow-up on the Steno-2 randomised trial. Diabetologia 2016; 59(11): 2298–2307. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–016–4065–6>.
6. Drucker DJ. GLP-1 physiology informs the pharmacotherapy of obesity. Mol Metab 2022; 57: 101351. Dostupné z DOI: <http://dx.doi.org/10.1016/j.molmet.2021.101351>.
7. Nissen SE, Wolski K. Effect of rosiglitazone on the risk of mycardial infarction and death from cardiovascular causes. N Engl J Med 2007; 356(24): 2457–2471. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa072761>.
8. Heerspink HJL, Perkins BA, Fitchett DH et al. Sodium glucose cotransporter 2 inhibitors in the treatment of diabetes mellitus: cardiovascular and kidney effects, potential mechanisms, and clinical applications. Circulation 2016; 134(10): 752–772. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.116.021887>.
9. [UK Prospective Diabetes Study (UKPDS) Group]. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes. Lancet 1998; 352(9131): 854–865.
10. Zinman B, Wanner C, Lachin JM et al. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med 2015; 373(22): 2117–2128. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1504720>.
11. [Nuffield Department of Population Health Renal Studies Group and SGLT2 inhibitor Meta-Analysis Cardio-Renal Trialists′ Consortium]. Impact of diabetes on the effects of sodium glucose co-transporter-2 inhibitors on kidney outcomes: collaborative meta-analysis of large placebo-controlled trials. Lancet 2022; 400(10365): 1788–1801. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(22)02074–8>.
12. Marso SP, Daniels GH, Brown-Frandsen K et al. Liraglutide and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2016; 375(4): 311–322. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1603827>.
13. Marso SP, Bain SC, Consoli A et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2016; 375(19): 1834–1844. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1607141>.
14. Sattar N, Yee MMY, Kristensen SL et al. Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with type 2 diabetes: a systematic review and meta-analysis of randomised trials. Lancet Diabetes Endocrinol 2021; 9(10): 653–662. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(21)00203–5>.
15. Dhatariya K, Bain SC, Buse JB et al. The impact of liraglutide on diabetes-related foot ulceration and associated complications in patients with type 2 diabetes at high risk for cardiovascular events: Results from the LEADER trial. Diabetes Care 2018; 41(10): 2229–2235. Dostupné z DOI: <http://dx.doi.org/10.2337/dc18–1094>.
16. Vaduganathan M, Docherty K, Claggett BL et al. SGLT2 inhibitors in patients with heart failure: a comprehensive meta-analysis of five randomised trials. Lancet 2022; 400(10354): 757–767. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(22)01429–5>.
17. Buse J, Bain SC, Mann JF et al. [LEADER Trial Investigators]. Cardiovascular risk reduction with liraglutide: an explotatory mediation analysis of the LEADER trial. Diabetes Care 2020; 43(7): 1546–1552. Dostupné z DOI: <http://dx.doi.org/10.2337/dc19–2251>.
18. Rubino MR, Greenway FL, Khalid U et al. [STEP 8 Investigators]. Effect of weekly semagludited vs dialy liraglutide on body weight in adults with overweight or obesity without diabetes. The STEP 8 randomized clinical trial. JAMA 2022; 327(2): 138–150. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2021.23619>.
19. Davies M, Faerch L, Jeppesen OK et al. Semaglutide 2.4 mg once a week in adults with overweight or obesity, and type 2 diabetes (STEP 2): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2021; 397(10278): 971–984. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(21)00213–0>.
20. Jastreboff AM, Aronne LJ, Ahmad N et al. Tirzepatide once weekly for the treatment of obesity. N Engl J Med 2022; 387(3): 205–216. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa2206038>.
21. Rosenstock J, Wysham C, Frías JP et al. Efficacy and safety of a novel dual GIP and GLP-1 receptor agonist tirzepatide in patients with type 2 diabetes (SURPASS-1): a double blind, randomised, phase 3 trial. Lancet 2021; 398(10295): 143–155. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(21)01324–6>.
22. Carlsson LMS, Sjöholm K, Jacobson P et al. Life expactancy after bariatric surgery in the Swedish Obese Subjects Study. N Engl J Med 2020: 383(16): 1535–1543. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa2002449>.
23. Tkáč I, Kimball BP, Lewis G et al. The severity of coronary atherosclerosis in type 2 diabetes mellitus is related to the number of circulating triglyceride-rich lipoprotein particles. Arterioscler Thromb Vasc Biol 1997; 17(12): 3633–3638. Dostupné z DOI: <http://dx.doi.org/10.1161/01.atv.17.12.3633>.
24. Ginsberg HN, Packard CJ, Chapman MJ et al. Triglyceride-rich lipoproteins and their remnants: metabolic insights, role in atherosclerotic cardiovascular disease, and emerging therapeutic strategies – a consensus statement from the European Atherosclerotic Society. Eur Heart J 2021; 42(47): 4791–4806. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehab551>.
25. Sabatine MS, Leiter LA, Wiviott SD et al. Cardiovascular safety and efficacy of the PCSK9 inhibitor evolocumab in patients with and without diabetes and the effect of evolocumab on glycaemia and risk of new-onet diabetes: a prespecified analysis of the FOURIER randomised controlled trial. Lancet Diabetes Endocrinol 2017; 5(12): 941–950. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(17)30313–3>.
26. Ray KK, Colhoun HM, Szarek M et al. Effects of alirocumab on cardiovascular and metabolic outcomes after acute coronary syndrome in patients with or without diabetes: a prespecified analysis of the ODYSSEY OUTCOMES randomised controlled trial. Lancet Diabetes Endocrinol 2019; 7(8): 618–628. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(19)30158–5>.
27. Keech A, Simes RJ, BarterP et al. [FIELD Study Investigators]. Effect of long-term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial. Lancet 2005; 366(9500): 1849–1861. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(05)67667–2>.
28. Ginsberg HN, Elam MB, Lovato LC et al. [Accord Study Group]. Effects of combination lipid therapy in type 2 diabetes mellitus. N Engl J Med 2010; 362(17): 1563–1574. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1001282>.
29. Das Pradhan A, Glynn RJ, Fruchart J-C et al. Triglyceride lowering with pemafibrate to reduce cardiovascular risk. N Engl J Med 2022; 387(21): 1923–1934. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa2210645>.
30. Bhatt DL, Steg PG, Miller M et al. Cardiovascular risk reduction with icosapent etyl for hypertriglyceridemia. N Engl J Med 2019; 380(1): 11–22. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1812792>.
31. Dahl K, Brooks A, Almazedi F et al. Oral semaglutide improves postprandial glucose and lipid metabolism, and delays gastric emptying, in subjects with type 2 diabetes. Diabetes Obes Metab 2021; 23(7): 15904–1603. Dostupné z DOI: <http://dx.doi.org/10.1111/dom.14373>.
32. Bergmark BB, Marston NA, Bramson CR et al. Effet of vupanorsen on non-high-density lipoprotein cholesterol levels in statin-treated patients with elevated cholesterol: TRANSLATE-TIMI 70. Circulation 2022; 145(18): 1377–1386. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.122.059266>.,
Štítky
Diabetologie Endokrinologie Interní lékařstvíČlánek vyšel v časopise
Forum Diabetologicum

2023 Číslo 1
Nejčtenější v tomto čísle
- Predpisovanie kyseliny alfa-lipoovej pacientom s diabetickou neuropatiou v súlade s princípmi medicíny dôkazov
- Specifika farmakoterapie u obézních pacientů
- Obezita ako podhubie kardio-nefro-hepato-metabolických ochorení
- Psychologická péče o pacienty před a po bariatrické/ metabolické operaci
