Farmakologický manažment diabetickej dyslipidémie
Pharmacological management of diabetic dyslipidaemia
Cardiovascular diseases are extremely common in type 2 diabetics. This is due to the presence of characteristic atherogenic dyslipidemia, which significantly contributes to increased cardiovascular risk. Atherogenic dyslipidemia is associated with a worse cardiovascular prognosis, but its management, especially treatment options that lead to a decrease in residual risk, are often ignored in clinical practice. The primary goal of treating diabetic dyslipidemia is to reduce LDL-cholesterol by statins, and diabetics not achieving LDL-cholesterol targets can add ezetimibe to treatment, which further reduces not only LDL-cholesterol but also cardiovascular risk. For diabetic patients achieving LDL-cholesterol targets with statin and/or ezetimibe with atherogenic dyslipidemia addition of fenofibrate leads to further improvement of lipid abnormalities with possible risk reduction. Treatment with fenofibrate is also very useful in diabetic patients with microvascular complications. A new promises for diabetics at very high cardiovascular risk are PCSK9 inhibitors. The management of atherogenic dyslipidemia, in addition to primary LDL-cholesterol management, presents a higher chance of reducing residual cardiovascular risk in an increasingly large group of type 2 diabetics.
Key words:
atherogenic dyslipidemia, cardiovascular disease, ezetimibe, fenofibrate, PCSK9 inhibitors, pemafibrate, statins
Autoři:
Ľubomíra Fábryová
Působiště autorů:
Metabol KLINIK s. r. o., Ambulancia pre diabetológiu, poruchy látkovej premeny a výživy, Bratislava
Vyšlo v časopise:
Forum Diab 2017; 6(3): 155-163
Kategorie:
Hlavná téma
Souhrn
Kardiovaskulárne ochorenia sa u diabetikov 2. typu vyskytujú extrémne často. Dôvodom okrem iného je aj prítomnosť charakteristickej aterogénnej dyslipidémie, ktorá významne prispieva ku zvýšenému kardiovaskulárnemu riziku. Aterogénna dyslipidémia je asociovaná s horšou kardiovaskulárnou prognózou, avšak jej manažment, najmä možnosti liečby, ktoré vedú k poklesu reziduálneho rizika, často v klinickej praxi ignorujeme. Primárnym cieľom liečby dyslipidémie u diabetikov je redukcia LDL-cholesterolu (LDL-C) statínmi, u diabetikov nedosahujúcich cieľové hodnoty pre LDL-C môžeme do liečby pridať ezetimib, ktorý ďalej znižuje nielen LDL-C, ale aj kardiovaskulárne riziko. U diabetikov dosahujúcich ciele pre LDL-C statínom a/alebo ezetimibom, ale s prítomnou aterogénnou dyslipidémiou asociovanou s vysokým reziduálnym rizikom vedie pridanie fenofibrátu k ďalšej úprave lipidových abnormalít s možnou redukciou rizika. Liečba fenofibrátom je veľmi užitočná aj u diabetikov s mikrovaskulárnymi komplikáciami. Novým prísľubom pre diabetikov vo veľmi vysokom kardiovaskulárnom riziku sú PCSK9-inhibítory. Manažment aterogénnej dyslipidémie, popri manažmente primárneho cieľa – LDL-C, predstavuje vyššie šance v redukcii reziduálneho kardiovaskulárneho rizika v čoraz početnejšej skupine diabetikov 2. typu.
Kľúčové slová:
aterogénna dyslipidémia, ezetimib, fenofibrát, kardiovaskulárne ochorenie, PCSK9-ihibítory, pemafibrát, statíny
Úvod
Napriek obrovským pokrokom v pochopení a v liečbe rizikových faktorov, kardiovaskulárne (KV) ochorenia ostávajú stále vedúcou príčinou morbidity a mortality u dospelých pod 75 rokov v Európe [1]. Tradičnými rizikovými faktormi pre KV-ochorenia sú vek, mužské pohlavie, rodinná predispozícia, fajčenie, nedostatok pohybovej aktivity, obezita, artériová hypertenzia, vysoké hodnoty LDL-cholesterolu (LDL-C) a diabetes mellitus 2. typu (DM2T).
KV-ochorenia sa u diabetikov 2. typu vyskytujú extrémne často. Dve tretiny až tri štvrtiny diabetikov nakoniec zomiera na kardiovaskulárne a cerebrovaskulárne príhody alebo ich následky.
Diabetici majú 2–4 násobne vyššie riziko rozvoja KV-ochorení, cievnych mozgových príhod a úmrtia na kardiovaskulárne a cerebrovaskulárne ochorenia v porovnaní s nediabetikmi. Toto dramatické zvýšenie KV-rizika nedokážeme v plnom rozsahu vysvetliť pomocou vyššie uvedených tradičných rizikových faktorov. Do hry vstupujú aj ďalšie ako napríklad protrombotický stav, rozdiely v zložení lipoproteínových častíc asociované s inzulínovou rezistenciou a reprezentované aterogénnou dyslipidémiou.
Aterogénna dyslipidémia
DM2T je spojený s charakteristickou dyslipidémiou (aterogénnou dyslipidémiou, diabetickou dyslipidémiou, non-LDL-dyslipidémiou, lipidovou triádou), ktorá významne prispieva ku zvýšenému KV-riziku a vo väčšine prípadov predchádza rozvoju hyperglykémie. Dalo by sa povedať, že porucha metabolizmu lipidov je v niektorých ohľadoch viac v centre patogenézy DM, ako porucha inzulínovej sekrécie, aj keď táto je absolútnou podmienkou pre rozvoj hyperglykémie [2].
Aterogénna dyslipidémia je asociovaná s horšou KV-prognózou, avšak jej manažment, najmä možnosti liečby, ktoré vedú k poklesu reziduálneho KV-rizika často v klinickej praxi ignorujeme [3].
Vysoko aterogénny lipidový profil u diabetikov 2. typu je charakterizovaný zvýšenou koncentráciou triacylglycerolov (TAG), nízkymi hodnotami HDL-cholesterolu (HDL-C) a prítomnosťou malých denzných (md) LDL-častíc s relatívne normálnymi alebo ľahko zvýšenými koncentráciami LDL-C. Ďalšie lipidové abnormality typické pre diabetickú dyslipidémiu predstavujú kvalitatívne zmeny v zložení HDL-častíc a v kumulácii lipoproteínov bohatých na triacylglyceroly (remnantné chylomikróny a remnantné častice). VLDL remnantné VLDL-častice sa premietajú do vyšších hladín non-HDL-cholesterolu (non-HDL-C) a apolipoproteínu (apo) B100.
Tieto lipidové abnormality sú spojené s rôznymi patofyziologickými mechanizmami. Zvýšená aktivita CETP (cholesterylester transferového proteínu), ktorý má za úlohu sprostredkovať výmenu TAG z VLDL-častíc do LDL-častíc a esterov cholesterolu (CE) z LDL-častíc do VLDL-častíc vedie k vzniku na cholesterol bohatých aterogénnych remnantných VLDL-častíc a LDL-častíc bohatých na TAG. TAG sú následne z LDL-častíc masívne odhydrolyzovávané lipoproteínovou lipázou (LPL) alebo hepatálnou lipázou (HL) za vzniku mdLDL-častíc.
Podobným mechanizmom vznikajú aj mdHDL-častice. Pri zvýšenej aktivite CETP dochádza ku výmene TAG a CE medzi VLDL- a HDL-časticami za vzniku na TAG bohatých HDL-častíc, TAG z týchto častíc sú odhydrolyzovávané HL za vzniku mdHDL-častíc, ktoré strácajú svoju kardioprotektivitu. Na TAG bohaté HDL-častice podliehajú ďalšej modifikácii, ktorá vedie ku oddeleniu štrukturálne zaujímavého apoliproteínu (apo) AI (je podstatne rýchlejšie odbúravaný ako v spojení s HDL-časticou). Jedným z miest vylučovania apoAI sú obličky, výsledkom je redukcia apoAI, ako aj redukcia počtu HDL-častíc.
Pokles HDL-cholesterolu je spojený s výraznejšou redukciou HDL2- ako HDL3-častíc. Táto alterácia je spojená s endotelovou dysfunkciou, porušením reverzného transportu cholesterolu a poklesom antiaterogénneho potenciálu HDL-častíc. Malé denzné LDL-častice sú na druhej strane aterogénnejšie, ľahšie penetrujú cez stenu endotelu, majú vyššiu afinitu k proteoglykanom v intime, sú náchylnejšie na oxidáciu a sú spájané s vyššou syntézou tromboxanu A2 [4].
Aterogénnu dyslipidémiu charakterizuje súbor kvantitatívnych i kvalitatívnych zmien v metabolizme lipidov a lipoproteínov, ktoré vedú ku zvýšenej aterogenicite plazmy:
- zvýšená koncentrácia na triacylglyceroly (TAG) a apolipoproteín CIII (apoCIII) bohatých veľkých VLDL (VLDL1) častíc – pri rutínnom laboratórnom vyšetrení zisťujeme zvýšené hodnoty TAG
- kvalitatívne zmenené mdLDL-častice so zvýšenou koncentráciou apoB pri kvantitatívne normálnych alebo ľahko zvýšených hodnotách LDL-C
- kvantitatívne a kvalitatívne zmeny HDL-C (znížené koncentrácie cholesterolu transportovaného v HDL-časticiach, vznik mdHDL-častíc so stratou kardioprotektivity)
- zvýšená koncentrácia remnantných lipoporoteínových častíc (remnantných chylomikrónov a IDL-častíc)
- prítomnosť postprandiálnej hyperlipidémie
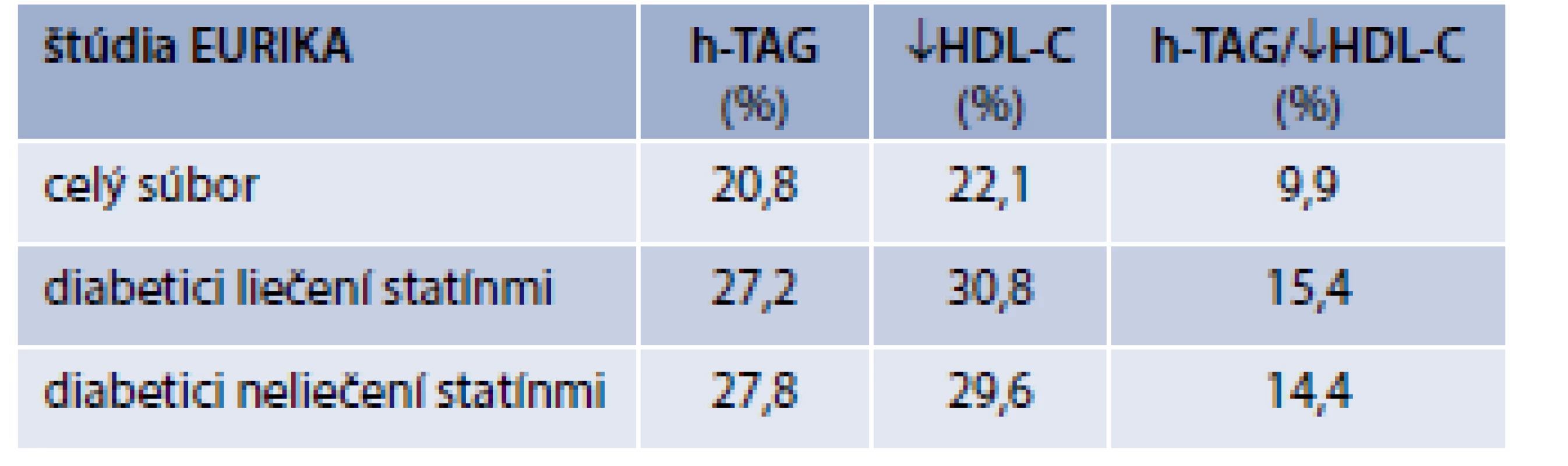
Aj keď prevalencia aterogénnej dyslipidémie nie je exaktne známa, informácie nám neustále pribúdajú [4]. Najnovšie údaje prináša observačná štúdia EURIKA (European Study on Cardiovascular Risk Prevention and Management in Usual Daily Practice; n = 7 641, 51,6 % žien, ≥ 50 rokov, s najmenej jedným rizikovým KV-faktorom, bez anamnézy KV-ochorenia), ktorá jasne ukázala na existujúcu medzeru medzi vysokou prevalenciou a nízkou terapeutickou intervenciou pri dvoch základných znakoch aterogénnej dyslipidémie (hypertriacylglycerolémia a nízke hodnoty HDL-C) [5]. Diabetici 2. typu mali vyššiu prevalenciu aj vyššie hodnoty triacylglycerolov a/alebo nízke hodnoty HDL-C v porovnaní s nediabetikmi. Nebol štatisticky významný rozdiel medzi výskytom hypertriacylglycerolémie a/alebo nízkych hodnôt HDL-C medzi diabetikmi liečenými a neliečenými statínmi (tab. 1).
Cieľe hypolipidemickej liečby u diabetikov 2. typu podľa recentných odporúčaní
Súčasné publikované odborné odporúčania neudávajú uniformné ciele liečby diabetickej dyslipidémie.
Odporúčania American College of Cardiology/American Heart Association
V roku 2013 sa v odporúčaniach ACC/AHA (American College of Cardiology/American Heart Association) udiala zmena v stratégii manažmentu dyslipidémií [6]. Od predchádzajúcich sa odlišujú tým, že nešpecifikujú liečebné ciele pre pacientov na základe ich KV-rizika, skôr určujú použitie „statínových“ režimov. Intenzifikovanej statínovej liečbe zodpovedná podávanie atorvastatínu 40–80 mg/deň alebo rosuvastatínu 20–40 mg/deň. Štandardnej statínovej liečbe zodpovedná podávanie atorvastatínu 10–20 mg/deň, fluvastatínu 80 mg/deň, lovastatínu 40 mg/deň, pravastatínu 40–80 mg/deň, rosuvastatínu 5–10 mg/deň, simvastatínu 20–40 mg/deň alebo pitavastatínu 2–4 mg/deň). Intenzifikovaná statínová liečba je odporúčaná diabetikom vo veku 40 až 75 rokov s 10-ročným rizikom rozvoja aterosklerotického KV-ochorenia (Atherosclerotic Cardiovascular Disease – ASCVD) ≥ 7,5 %, štandardná statínová liečba je odporúčaná diabetikom, ktorí nespĺňajú kritériá pre použitie intenzifikovanej statínovej liečby. Tieto odporúčania nepodporujú sledovanie pacientov s cieľom posúdiť ich odpoveď na liečbu statínmi, neurčujú ďalšie non-LDL-C ciele, ako aj možnosti kombinácie s nestatínovými hypolipidemikami.
V roku 2016 bol publikovaný ďalší AHA/ACC konsenzus, ktorý zahŕňa už aj terapeutické ciele (percentuálna redukcia LDL-C), ako aj možnosti použitia nestatínových hypolipidemík [7].
Iba malé percento 40–75-ročných diabetikov s LDL-C 1,8–4,9 mmol/l má 10-ročné riziko ASCVD < 7,5 % bez prítomnosti ďalších rizikových faktorov, napr. retinopatia, chronické obličkové ochorenie, albuminúria alebo zvýšený lipoproteín (a) – Lp(a), subklinická ateroskleróza. V súčasnosti máme k dispozícii veľké množstvo dôkazov pre použitie štandardnej statínovej liečby v tejto populácii diabetikov.
Veľká väčšina diabetikov má však 10-ročné riziko ASCVD ≥ 7,5 % alebo prítomné ďalšie rizikové faktory. Táto skupina diabetikov má byť liečená intenzifikovanou statínovou liečbou s cieľom dosiahnuť ≥ 50% pokles LDL-C alebo LDL-C < 2,6 mmol/l (non-HDL-C < 3,4 mmol/l). Intenzifikovaná statínová liečba je liečbou voľby u diabetikov s KV-ochorením (pacienti s veľmi vysokým rizikom), cieľom je dosiahnuť hodnotu LDL-C < 1,8 mmol/l.
U pacientov nedosahujúcich uvedené liečebné ciele sa zameriavame na intenzívnejšiu modifikáciu životného štýlu a kontrolu adherencie k statínovej liečbe. Ak po tejto intervencii nie je stále adekvátna odpoveď na liečbu, pristupujeme k zvýšeniu dávky statínov. Pokiaľ aj po titrácii dosiahneme < 50% pokles LDL-C (alebo LDL-C ostáva > 2,6 mmol/l alebo non-HDL-C > 3,4 mmol/l) iniciujeme kombináciu statínu s nestatínovým hypolipidemikom. Takýto postup využívame najmä v prípade nedostatočnej odpovede na liečbu u diabetikov vo vysokom alebo veľmi vysokom riziku [7].
Odporúčania American Diabetes Association
ADA (American Diabetes Association) odporúča hypolipidemickú liečbu u väčšiny diabetikov okrem diabetikov mladších ako 40 rokov bez ďalších rizikových faktorov. Diabetici vo veku > 40 rokov by mali byť liečení štandardnou statínovou liečbou. Pacienti vo veku 40–75 rokov s jedným rizikovým KV-faktorom môžu byť liečení štandardnou alebo intenzifikovanou statínovou liečbou. Diabetici s väčším počtom rizikových faktorov alebo s prítomným KV-ochorením by mali byť liečení intenzifikovanou statínovou liečbou [8].
Odporúčania European Cardiology Society
Európske odporúčania ESC (European Cardiology Society) publikované v roku 2016 zamerané na prevenciu KV-ochorení v klinickej praxi viac alebo menej súhlasia s vyššie uvedenými odporúčaniami. Hypolipidemická liečba (statíny) je odporúčaná u všetkých diabetikov > 40 ročných a môže byť použitá aj u mladších diabetikov so signifikantne zvýšeným rizikom založeným na prítomnosti mikrovaskulárnych komplikácií alebo mnohopočetných KV-rizikových faktorov. U pacientov vo veľmi vysokom riziku (prítomnosť KV-ochorenia, DM s orgánovým poškodením napr. proteinúria, fajčenie, závažná hypercholesterolémia alebo artériová hypertenzia, závažné chronické obličkové ochorenie alebo vypočítané SCORE ≥ 10 %) je cieľom dosiahnuť LDL < 1,8 mmol/l alebo prinajmenšom 50% redukciu pokiaľ je bazálny LDL-C medzi hodnotami 1,8 až 3,5 mmol/l. U pacientov vo vysokom riziku (markantne zvýšený 1 rizikový faktor napr. celkový cholesterol > 8 mmol/l alebo krvný tlak ≥ 180/110 mm Hg, mierne chronické obličkové ochorenie alebo SCORE ≥ 5 % a < 10 %) je cieľom dosiahnuť hodnotu LDL-C < 2,6 mmol/l alebo redukovať LDL-C prinajmenšom o 50 % pri bazálnom LDL-C medzi hodnotami 2,6 a 5,2 mmol/l [9].
Odporúčania European Atherosclerosis Society
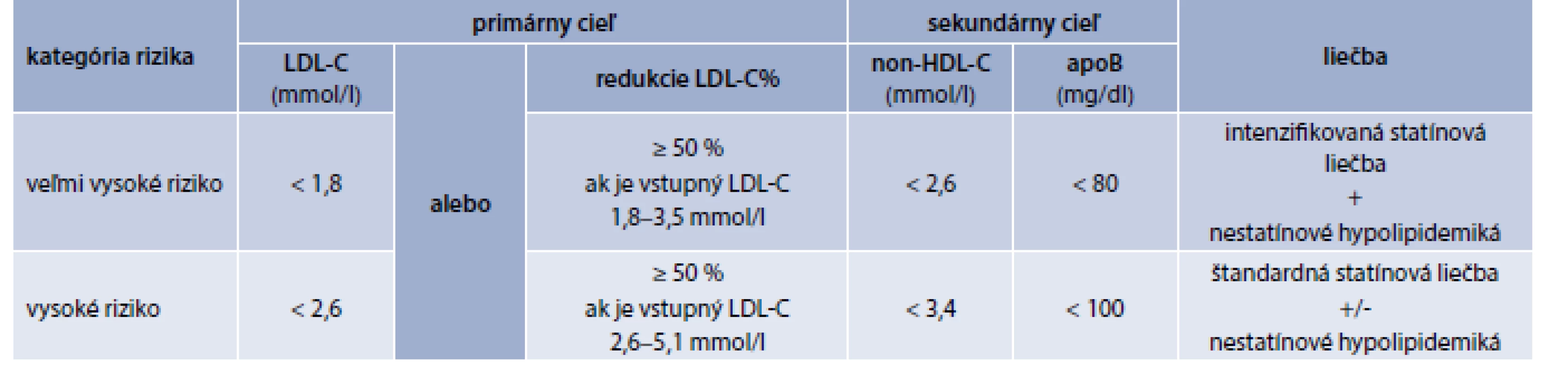
V odporúčaniach ESC/EAS (European Atherosclerosis Society) pre manažment dyslipidémií u diabetikov 2. typu sú uvedené nasledovné ciele: u pacientov s chronickým KV-ochorením alebo chronickým ochorením obličiek podobne ako u diabetikov bez KV-ochorenia > 40 ročných s jedným alebo viacerými inými KV-rizikovými faktormi alebo markermi orgánového poškodenia sú odporúčané cieľové hodnoty primárne pre LDL-C < 1,8 mmol/l a sekundárnym cieľom sú non-HDL-C < 2,6 mmol/l a apoB < 80 mg/dl. U ostatných diabetikov, bez rizikových faktorov a/alebo prítomnosti poškodenia cieľových orgánov je primárnym cieľom LDL-C < 2,6 mmol/l, sekundárnymi cieľmi sú non-HDL-C < 3,4 mmol/l a apoB < 100 mg/dl. Statíny sú liekmi prvej voľby, pokiaľ nie sú dosiahnuté cieľové hodnoty do terapie je možné pridať ezetimib (tab. 2) [10].
Terapeutické možnosti manažmentu diabetickej dyslipidémie
Ovplyvnenie životného štýlu
Snaha o zmenu životného štýlu je základom liečby akejkoľvek poruchy metabolizmu lipidov a lipoproteínov, o to viac to platí pre aterogénnu dyslipidémiu. Súčasťou zmeny životného štýlu je dodržiavanie diétnych opatrení, pohybovej aktivity a dosiahnutie alebo udržanie „zdravej“ telesnej hmotnosti. Takéto opatrenia sa ťažko implementujú, adherencia býva väčšinou nízka, ale treba povedať, že sú vysoko efektívne v ovplyvnení mnohých zložiek aterogénnej dyslipidémie. Vyššie uvedené opatrenia vedú k zlepšeniu inzulínovej senzitivity a všeobecne metabolického statusu, čo vedie k zlepšeniu lipidového profilu. Napriek týmto pozitívam nefarmakologická liečba nepreukázala vplyv na redukciu KV-endpointov [11].
Liečba statínmi
Liečba statínmi vedie k signifikantnej redukcii koncentrácie LDL-C a súčasné štandardy prevencie kardiovaskulárnych a cerebrovaskulárnych ochorení ju považujú za prvolíniovú liečbu diabetickej dyslipidémie. Tento fakt je podporený mnohými randomizovanými klinickými štúdiami (randomized clinical trials – RCT), ktoré dokázali signifikantnú redukciu KV-príhod pri liečbe statínmi u diabetikov.
Do štúdie HPS (Heart Protection Study) bolo randomizovaných 5 963 diabetikov 2. typu a 14 573 nediabetikov s okluzívnym arteriálnym ochorením na podávanie simvastatínu v dávke 40 mg/deň alebo placeba. Liečba simvastatínom viedla k poklesu LDL-C o 1,0 mmol/l v porovnaní s placebom, čo sa premietlo do signifikantnej 25 % redukcie počtu veľkých koronárnych príhod, cievnych mozgových príhod a revaskularizácií. V podskupine diabetikov bol zaznamenaný 22% signifikantný pokles veľkých KV-príhod. Podobný pokles veľkých KV-príhod bol dokázaný aj u diabetikov s relatívne nízkymi vstupnými hodnotami LDL-C (< 3,0 mmol/l; -27 %, 95% CI 13–40, p = 0,0007) [12].
Štúdia CARDS (Collaborative Atorvastatin Diabetes Study) randomizovala 2 838 diabetikov vo veku 40–75 rokov s hodnotami LDL-C < 4,14 mmol/l na liečbu atorvastatínom 10 mg/deň alebo placebo. Liečba atorvastatínom signifikantne redukovala veľké KV-príhody o 37 % (95% CI 17–52, p = 0,001), akútne KV-príhody o 36 % (95% CI 9–55, p < 0,05), koronárne revaskularizácie o 31 % (95% CI 16–59, p < 0,05) a cievne mozgové príhody o 48 % (95% CI 11–69, p < 0,05), bola zaznamenaná aj takmer signifikantná redukcia počtu úmrtí (-27%, p = 0,059) [13].
Metaanalýza štúdií zameraných na monoterapiu statínmi u 18 686 diabetikov poukázala na 9% redukciu celkovej mortality a 21% redukciu incidencie veľkých KV-príhod pri poklese LDL-C o 1 mmol/l [14]. Podobný výsledok potvrdzuje metaanalýza statínových štúdií u nediabetikov ako v primárnej, tak i sekundárnej prevencii [15].
Liečba statínmi je spojená s nízkym výskytom závažných nežiaducich udalostí. Klinickí lekári sa najčastejšie obávajú výskytu myopatie alebo rabdomyolýzy. Ale tieto nežiaduce udalosti sú veľmi raritné. Pozornosť si vyžadujú pacienti s relatívne zvýšeným rizikom výskytu svalových nežiaducich udalostí (vyšší vek, pacienti s chronickým obličkovým ochorením, neliečenou alebo subklinickou hypotyreózou). Pozornosť treba venovať aj liekom, ktoré môžu interagovať so statínmi (zosilňovať alebo zoslabovať ich efekt). Nežiaduce udalosti spojené so zvýšením hepatálnych parametrov bývajú taktiež veľmi raritné. Súčasné odporúčania vôbec neodporúčajú kontrolné merania transamináz u pacientov liečených statínmi.
Terapia statínmi je spojená aj s nepriaznivým efektom na homeostázu glukózy. Metaanalýza údajov od 91 140 pacientov poukázala, že liečba statínmi môže zvyšovať riziko rozvoja novovzniknutého diabetes mellitus o 9 %. Avšak toto riziko sa líši v rámci používaných statínov. Na druhej strane si musíme uvedomiť, že riziko rozvoja nového DM je nízke oproti benefitu vyplývajúceho z redukcie KV-príhod. Pozor si musíme dávať najmä u pacientov s nízkym KV-rizikom, ale s rizikovými faktormi rozvoja DM (prediabetes) [16].
Štúdie u diabetikov tiež poukázali na mierne poškodenie metabolizmu karbohydrátov. V štúdii CARDS bola zaznamenané ľahké zvýšenie progresie glykémie definované ako nárast glykovaného hemoglogínu (HbA1c) ≥ 0,5 % alebo nutnosť intenzifikácie liečby DM. Celkový efekt statínovej liečby na HbA1c bol jeho nárast o 0,14 % (95% CI 0,08–0,21). Avšak tento efekt atorvastatínu na HbA1c sa nezvyšoval časom, nepredikoval prípadné KV-príhody a nemal vplyv na efekt atorvastatínu na pokles KV-rizika [17].
Metaanalýza údajov od 9 696 diabetikov liečených statínmi poukázala na malé zvýšenie HbA1c o 0,12 % (95% CI 0,04–0,20, p = 0,003) oproti placebovej skupine. Toto nás však neoprávňuje k vysadeniu statínovej liečby u diabetikov, ktorí z tejto terapie signifikantne profitujú poklesom KV-príhod [18].
Liečba kombináciou statínu s ezetimibom
Mechanizmus účinku ezetimibu spočíva v selektívnej inhibícii resorpcie cholesterolu a iných sterolov v tenkom čreve. Blokuje špecificky proteín tzv. Niemann-Pick C1 Like-1-transportér (NPC1L-1) nachádzajúci sa v membránach enterocytov kartáčikového lemu jejúna. Účinkom tejto blokády dochádza k poklesu cholesterolu v chylomikrónoch a tým k zníženiu jeho prísunu do pečene s následným zvýšením expresie LDL-receptorov (LDLR) na povrchu pečeňovej bunky a zvýšeným vychytávaním LDL-C z plazmy. Znížený prísun cholesterolu z tenkého čreva vedie k zníženej inkorporácii cholesterolu do VLDL-častíc, čo pečeň kompenzuje zvýšenou endogénnou tvorbou cholesterolu v pečeni.
Naopak pri podaní statínu v monoterapii síce dochádza ku zníženiu endogénnej syntézy cholesterolu v pečeni, ale súčasne dochádza k významnému zvýšeniu resorpcie cholesterolu v čreve. Na týchto údajoch stojí duálna inhibícia, ktorej cieľom je ovplyvniť ako syntézu, tak aj spätnú resorpciu cholesterolu z čreva.
Kombinácia statínu s ezetimibom ovplyvňujúca nielen prísun cholesterolu z čreva, ale aj endogénnu tvorbu cholesterolu pečeňou (potencovanie duálneho efektu) sa javí ako veľmi dôležitá u diabetikov 2. typu. Pridanie 10 mg ezetimibu k statínu vedie podľa mnohých klinických štúdii k ďalšej redukcii LDL-C o 20–25 % (pri zdvojnásobení dávky statínu je prídavná redukcia LDL-C iba 5–7 %).
Ezetimib tiež vedie v menšom rozsahu ku zlepšeniu TAG a koncentrácií HDL-C a vykazuje aj pleiotropné účinky, ako napríklad redukciu počtu aterogénnych mdLDL-častíc.
Efekt pridania ezetimibu k statínu na KV riziko bol sledovaný v štúdii IMPROVE-IT (IMProved Reduction of Outcomes: Vytorin Efficacy International Trial), do ktorej bolo randomizovaných 18 144 pacientov hospitalizovaných pre akútny koronárny syndróm buď na kombináciu ezetimib/simvastatín (10/40 mg) alebo placebo/simvastatín (40 mg). Kombinácia ezetimib/simvastatín viedla k výraznejšej redukcii LDL-C v porovnaní s monoterapiou simvastatínom (1,4 vs 1,8 mmol/l p < 0,001). Kombinácia ezetimib/simvastatín viedla k väčšej redukcii incidencie primárnych end pointov v porovnaní s monoterapiou simvastatínom (32,7 % vs 34,7 %, HR 0,936, 95% CI 0,89–0,99, p = 0,016). Štúdia IMPROVE-IT dokázala, že ďalšie zníženie LDL-C vedie k ďalšej redukcii KV-rizika u vysokorizikových pacientov a aj nestatínová hypolipidemická liečba má svoje opodstatnenie v manažmente KV-rizika. Subanalýza diabetickej populácie ukázala, že kombinácia ezetimib/simvastatín je spojená s redukciou absolútneho rizika o 5,5 % (HR 0,86, 95% CI 0,78–0,94) v primárnych endpointoch v porovnaní s monoterapiou simvastatínom. U nediabetikov bol zistený nesignifikantný rozdiel (HR 0,98, 95% CI 0,91–1,04) [19].
Výskyt nežiaducich udalostí pri kombinácii ezetimibu so statínom je nízky a táto kombinácia je vo všeobecnosti bezpečná pre diabetikov, nedochádza k ovplyvneniu parametrov metabolizmu uhľohydrátov [20].
Liečba kombináciou statínu s fenofibrátom
Fibráty sú agonisty PPARa (peroxisome proliferator-activated receptors alfa). PPARa prostredníctvom fibrátov regulujú gény jednotlivých faktorov zapojených do metabolizmu lipidov a lipoproteínov. Stimuláciou génov zapojených do metabolizmu LPL, zvyšujú jej produkciu, čo vedie k zvýšenej lipolýze na TAG bohatých lipoproteínov, ako aj k zvýšenej oxidácii mastných kyselín. Inhibícia apoCIII vedie taktiež k zníženej koncentrácii lipoproteínov bohatých na TAG. Intervencia fibrátmi vedie k zmenám štruktúry aj veľkosti VLDL častíc. Znížením obsahu apoCIII sa znižuje aj obsah TAG vo VLDL-časticiach čo vedie k produkcii menších VLDL-častíc, ktoré menej interagujú s CETP. Tým sú generované väčšie LDL-častice, ktoré sú rozpoznávané klasickým LDL-receptorom. Expresia apoAV sprostredkovaná aktiváciou PPARa fibrátmi má tiež dramatický vplyv na pokles hladiny TAG. Aktivácia PPARa reguluje expresiu génov metabolizmu HDL-častíc (expresia génov apoAI, apoAII, expresia génu pre LPL, expresia SR-BI-receptora a ABCA-I-transportéra). Stimulácia expresie génov apoAI a apoAII vedie k zvýšeniu syntézy apoAI a apoAII, čo korešponduje so zvýšenou formáciou HDL-častíc. Stimulácia expresie génov pre ABCA-I-transportér (sprostredkuje eflux cholesterolu cez CERP – cholesterol efflux regulatory protein) a SR-BI-receptor (sprostredkuje vychytávanie a katabolizmus HDL-častíc) vedie k zvýšeniu reverzného transportu cholesterolu. V súčasnosti sa potvrdzujú aj tzv. pleiotropné účinky fibrátov (ovplyvnenie inzulínovej senzitivity, vplyv na progresiu inzulínovej rezistencie, ovplyvnenie endotelovej dysfunkcie, antitrombotické, protizápalové a antioxidačné účinky).
Významným účinkom fibrátov je redukcia TAG o 25–50 % a zvýšenie HDL-C o 15–25 %. Taktiež klesá množstvo cholesterolu vo frakcii VLDL, kým pokles cholesterolu v LDL-časticiach je menší (5–20 %) v závislosti od použitého fibrátu (fenofibrát spĺňa všetky uvedené atribúty). Z kvalitatívnych zmien je významný najmä pokles frakcie mdLDL-častíc a skrátenie trvania postprandiálnej lipémie. Napriek vyššie uvedenému vplyvu fibrátov na zložky diabetickej (aterogénnej) dyslipidémie sú výsledky klinických štúdií s rôznymi fibrátmi z pohľadu KV-prevencie menej impresívne [21].
Nedávno publikovaný systematický prehľad 13 fibrátových randomizovaných klinických štúdií svedčí o signifikantnom 12% efekte fibrátov v porovnaní s placebom na KV-ochorenia, ale nie o redukcii celkovej mortality alebo redukcii úmrtí na vaskulárne ochorenia [22]. Avšak metaanalýza fibrátových štúdií v skupine pacientov s aterogénnou dyslipidémiou poukázala na 35% pokles KV-príhod [23]. Liečba fenofibrátom dokáže viesť ku redukcii reziduálneho mikrovaskulárneho rizika u diabetikov 2. typu (diabetickej retinopatie, nefropatie) [24]. Niektoré práce poukazujú na fakt, že v kombinácii so statínmi, fibráty môžu eliminovať riziko zvýšenia glykémie spojeného so statínovou liečbou [25].
Potrebujeme však ďalšie klinické štúdie s precíznejšou selekciou pacientov s aterogénnou dyslipidémiou, ktoré by dokázali efekt buď samotných fibrátov alebo fibrátov v kombinácii so statínmi na morbiditné a mortalitné KV-endpointy.
Potentnejšie selektívne PPARa-modulátory (selective PPAR modulators – SPPARM) by mohli výraznejšie zredukovať TAG, ako aj mať lepší inzulín-senzitizujúci efekt, otázkou ostáva ich bezpečnosť. Tento rok bola iniciovaná (aj na Slovensku) veľká medzinárodná multicentrická štúdia PROMINENT (Pemafibrate to Reduce cardiovascular OutcoMes by reducing triglycerides IN diabetic patiENTs). Bude hodnotiť pemafibrát (SPPARM) v prevencii veľkých KV-príhod u vysokorizikových diabetikov (10 000 pacientov s TAG ≥ 2,26 mmol/l a HDL-C ≤ 1,03 mmol/l so statínovou liečbou) a snáď dá odpoveď na doposiaľ nezodpovedané otázky [26].
PCSK9-inhibítory
PCSK9 (proproteín konvertáza subtilizín-kexín 9) je proteín primárne syntetizovaný a secernovaný hepatocytmi, s dôležitou úlohou v homeostáze cholesterolu. Cirkulujúce PCSK9 sa viaže na LDL-receptor (LDL-R) .a zabraňuje jeho recyklácii na povrch pečeňovej bunky. Toto zníženie LDL-R vedie ku akumulácii LDL-častíc v plazme. Blokáda PCSK9-inhibítormi – monoklonálnymi protilátkami (alirokumab, evolokumab) umožňuje recykláciu LDL-R a razantné zníženie koncentrácie LDL-C (približne o 60 %) [27,28]. Tento rok boli publikované výsledky štúdie FOURIER (Futher cardiovascular OUTcomes Research with PCSK9 inhibition in subjects with Elevated Risk), ktorá nám priniesla „tvrdé“ endpointové morbiditno-mortalitné údaje. Primárny kompozitný endpoint (úmrtie z KV-príčin, infarkt myokardu, cievna mozgová príhoda, hospitalizácia pre nestabilnú angínu pectoris potreba koronárnej revaskularizácie) bol signifikantne viac znížený v evolokumabovej skupine (9,8 %) oproti placebovej skupine 11,3 %, čo predstavuje 15% redukciu. Sekundárne endpointy (KV-úmrtie, infarkt myokardu, cievna mozgová príhoda) sa objavili u 5,9 % pacientov liečených evolokumabom a u 7,4 % pacientov užívajúcich placebo, dokonca s 20% redukciou. Štúdia trvala len o niečo viac ako 2 roky, ale pozitívne je, že v 1. roku štúdie bola redukcia rizika primárneho (sekundárneho) endopointu 12% (16%) a v 2. roku štúdie redukcia narástla na 19 % (resp. 25 %) [29].
V súčasnosti máme k dispozícii údaje z rôznych línií výskumu o tom, že PCSK9 ovplyvňuje okrem LDL-C aj metabolizmus ostatných lipoproteínov, najmä lipoproteínov bohatých na TAG a ich remnantných častíc. Vzťah medzi PCSK9 a lipoproteínmi bohatými na TAG sa dá predpokladať na základe napr. korelácie medzi plazmatickými hladinami PCSK9 a markermi uhľohydrátového metabolizmu, ktoré sú úzko asociované s metabolizmom TAG. Z ďalších príkladov môžeme uviesť: efekt fibrátov znižujúcich TAG na plazmatickú hladinu PCSK9, efekt PCSK9 na postprandiálnu lipémiu, na biológiu tukového tkaniva, na produkciu apoB pečeňou a črevom, efekt PCSK9 nielen na LDL-R, ale aj na receptory ovplyvňujúce metabolizmu na TAG bohatých lipoproteínov a v neposlednom rade efekt inhibítorov PCSK9 na sérové hladiny TAG. Tieto mechanizmy nie sú ešte úplne objasnené, ale v každom prípade vzbudzujú nemalý záujem [30].
S dvomi PCSK9 inhibítormi (evolokumab, alirokumab) bol uskutočnený rozsiahly program klinických štúdií ODDYSEY (Observational Dutch Young Symptomatic StrokE studY), PROFICIO (Program to Reduce LDL-C and Cardiovascular Outcomes Following Inhibition of PCSK9 In Different POpulations) zameraný na rôzne populácie pacientov. Klinický výskum s bokocizumabom – SPIRE (Studies of PCSK9 Inhibition and the Reduction of Vascular Events) bol nedávno ukončený pre tvorbu autoprotilátok, ktoré viedli k poklesu účinnosti liečby.
Treba povedať, že žiadna zo štúdií s PCSK9 nebola robená špeciálne v populácii diabetikov. Avšak v rámci jednotlivých programov bolo zaradené veľké množstvo diabetikov, čo poskytuje dôkazy o ich účinnosti a bezpečnosti u týchto pacientov. Systematický prehľad u 10 000 účastníkov ukázal, že 87 % pacientov na alirokumabe a 98 % pacientov na evolokumabe dosiahlo cieľové hodnoty pre LDL-C v širokej populácii pacientov vrátane diabetikov.
Metaanalýza RCT porovnávala efekt evolokumabu, placeba a ezetimibu na lipidové parametre u 18–80-ročných pacientov diabetikov (n = 413) alebo nediabetikov (n = 1 119). U diabetikov viedol evolokumab k 60% redukcii LDL-C (95% CI 51–69) oproti placebu a 39% (95% CI 32–47) redukcii oproti ezetimibu. Redukcia LDL-C u nediabetikov bola 66% (95% CI 62–70) oproti placebu a 40% (95% CI 36–45) oproti ezetimibu. U diabetikov evolokumab oproti placebu viedol k signifikantnej redukcii non-HDL-C, celkového cholesterolu a Lp(a) a k signifikantnému nárastu HDL-C [31].
V štúdii OSLER-1 a OSLER-2 (Open-Label Study of Long-Term Evaluation against LDL Cholesterol 1 and 2) boli pacienti randomizovaní v pomere 2 : 1 na liečbu evolokumabom v kombinácii so štandardnou liečbou vs štandardná liečba. Zo 4 802 subjektov bolo 852 diabetikov, 2 432 bolo vo vysokom riziku rozvoja DM a 1 518 bolo v nízkom riziku rozvoja DM. Liečba evolokumabom v trvaniu 1 roka viedla k markantnej redukcii LDL-C vo všetkých skupinách a nemala žiadne merateľný efekt na glykemické parametre, vrátane rozvoja novovzniknutého DM v porovnaní so štandardnou liečbou [32].
Analýza účinnosti a bezpečnosti alirokumabu oproti placebu u pacientov s heterozygotnou familiárnou hypercholesterolémiou (FH) neadekvátne kontrolovaných na štandardnej hypolipidemickej liečbe (ODYSSEY) štúdie 3. fázy klinického skúšania (n = 4 974) v trvaní 24–104 týždňov skúmala efekt alirokumabu na homeostázu glukózy u nediabetikov. Špeciálne boli sledované nežiadúce udalosti vzniknuté vo vzťahu s DM a/alebo glykémiou nalačno a HbA1c vstupne a následne každých 12–24 týždňov. Mnohí pacienti užívali maximálne tolerované dávky statínov so známym diabetogénnym potenciálom. Pri vstupe do štúdie malo 37 % pacientov DM (vylúčení z následnej analýzy), 39,6 % malo prediabetes a 29,7 % bolo normoglykemických. HR pre nežiadúce udalosti vzniknuté vo vzťahu s DM bolo pre alirokumab 0,64 (95% CI 0,36–1,14) vs placebo a 0,55 (CI 0,22–1,41) oproti ezetimibu. HR pre prechod z prediabetu do novovzniknutého DM2T bolo pre alirokumab 0,90 (CI 0,63–1,29) vs. placebo a 1,10 (CI 0,57–2,12) vs. ezetimib. Počas celej analýzy neboli zaznamenané žiadne rozdiely v liečebných skupinách v priemernej zmene glykémie nalačno a HbA1c. Alirokumab nevedie k negatívnemu ovplyvňovaniu homeostázy glukózy u pacientov nediabetikov v porovnaní s placebom alebo ezetimibom [33].
PCSK9 inhibítory vedú k ďalšej významnej redukcii LDL-C a všeobecne zlepšujú lipidový profil u diabetikov. V súčasnosti platných odporúčaniach je uvedené, že v klinickej praxi máme využívať PCSK9 inhibítory u dospelých diabetikov s KV-ochorením a LDL-C ≥ 2,6 mmol/l popri modifikácii životného štýlu a maximálne tolerovanej hypolipidemickej liečbe (intenzifikovaná statínová liečba a ezetimib).
Farmakologický manažment zvýšenej koncentrácie mdLDL-častíc
Charakteristickou črtou diabetickej dyslipidémie je zvýšená koncentrácia mdLDL častíc napriek relatívne podobných alebo ľahko zvýšených koncentráciách LDL-C v porovnaní so všeobecnou populáciou. Malé denzné LDL-častice sú vysoko aterogénne, ľahšie prenikajú do subendotelového priestoru steny artérií, sú náchylné na oxidáciu a vychytávanie makrofágmi, urýchľujú formovanie penových buniek a potencujú endotelovú dysfunkciu. Tieto častice zvyšujú KV-riziko a mali by byť cieľom liečby u diabetikov [4].
Statín a/alebo ezetimib vedú k zníženiu koncentrácií mdLDL-častíc, ale nemenia distribúciu LDL-subfrakcií. U hypertriglyceridemických osôb rosuvastatín podobne ako ezetimib vedie k modifikácii distribúcie LDL-subfrakcií a zvyšuje veľkosť LDL-častíc.
Fenofibrát redukuje koncentráciu mdLDL-častíc a mení LDL-fenotyp – vedie k formovaniu veľkých, menej aterogénnych LDL-častíc. Ovplyvnenie ako kvantity, tak aj kvality LDL-častíc je sľubné pre redukciu KV rizika, avšak štúdie špecificky zamerané na tento efekt nám chýbajú. Alirokumab vedie k redukcii koncentrácie veľkých i malých LDL-častíc (nukleárna magnetická rezonančná spektroskopia) bez signifikantného ovplyvnenia veľkosti LDL-častíc. Pomocou ďalšej metódy (vertikálna autotoprofilová metóda) vedie podávanie alirokumabu k zníženiu obsahu cholesterolu v subfrakciách LDL1, LDL2 a LDL3–4. Výsledky prebiehajúcich klinických štúdií nám ukážu, či sa táto zmena v koncentrácii lipoproteínových častíc spolu s redukciou LDL-C indukovanou inhibíciou PCSK9 pretaví do ďalšieho klinického benefitu [34].
Budúcnosť ovplyvňovania aterogénnej dyslipidémie
Blízkou budúcnosťou pre ovplyvnenie aterogénnej dyslipidémie môžu byť nové CETP-inhibítory – anacetrapib (štúdia DEFINE – Details of the Determining the Efficacy and Tolerability of CETP Inhibition with Anacetrapib) a novší TA-8995 (štúdia TULIP – TA-8995: Its Use in Patients With Mild Dyslipidaemia).
Na začiatku klinického výskumu je anti-sense inhibícia apoCIII (podávaná injekčne raz do týždňa, v monoterapii alebo v kombinácii s fibrátmi) viedla u pacientov s hyperTAG nalačno k redukcii koncentrácií TAG o 70 % (v závislosti od dávky).
Ďalšou v poradí je farmakologická inhibícia ANGPTL3 (angiopoietin-like) a ANGPTL4, hypolipidemický efekt čaká na potvrdenie v klinických štúdiách.
V liečbe diabetes mellitus a dyslipidémie sa zdá byť sľubnou farmakologická inhibícia enzýmov konečných krokov biosyntézy TAG – diacylglycerol acyltransferázy (DGAT) a monoacylglycerol acyltransferázy (MGAT). Vo vývoji sú viaceré inhibítory DGAT1, dúfajme, že účinnejšie a bezpečnejšie.
Izoenzým selektívne inhibítory Acetyl-CoA karboxylázy (ACC) inhibujú lipogenézu a zvyšujú oxidáciu mastných kyselín, čo môže byť veľmi užitočné v liečbe diabetikov 2. typu, hyper-TAG a nealkoholovej steatohepatitídy. Zatiaľ ešte neboli skúšané v klinických štúdiách
Duálny modulátor dvoch hepatálnych enzýmov, ETC-1102 inhibuje ATP citrát lyázu a aktivuje AMPK (AMP aktivovanú proteín kinázu) v pečeni, ktorá inhibuje syntézu sterolov a mastných kyselín a urýchľuje oxidáciu mastných kyselín. ETC-1102 vedie k redukcii LDL-C nezávisle od hladín TAG, k poklesu apoB100, non-HDL-C, počtu LDL-častíc, znižuje zápalové markery, krvný tlak a telesnú hmotnosť. Avšak potrebujeme dlhodobé štúdie na potvrdenie jeho bezpečnosti, tolerability a účinnosti [4].
Záver
Napriek obrovskému úspechu dosiahnutému vďaka statínovej liečbe pri znižovaní LDL-C so súčasnou redukciou kardiovaskulárnej a cerebrovaskulárnej morbidity a mortality, ostáva reziduálne KV-riziko stále vysoké. Je to vďaka nárastu obezity a s ňou súvisiaceho nárastu počtu diabetikov 2. typu s charakteristickou aterogénnou dyslipidémiou.
Diabetes mellitus je asociovaný s vysokým KV-rizikom a primárnym cieľom hypolipidemickej liečby je redukcia LDL-C statínmi. Na základe výsledkov štúdie IMPROVE-IT u pacientov nedosahujúcich cieľové hodnoty pre LDL-C môžeme do liečby pridať ezetimib, ktorý ďalej znižuje nielen LDL-C, ale aj KV-riziko.
Na základe podskupinovej analýzy štúdie ACCORD (Action to Control Cardiovascular Risk in Diabetes) u pacientov dosahujúcich ciele pre LDL-C statínom a/alebo ezetimibom, ale s prítomnou aterogénnou dyslipidémiou asociovanou s vysokým reziduálnym rizikom, pridanie fenofibrátu vedie k ďalšej úprave lipidových abnormalít a možnej redukcii KV-rizika. Liečba fenofibrátom je veľmi užitočná aj u pacientov s diabetickou retinopatiou.
PCSK9-inhibítory vedú k ďalšej redukcii LDL-C a sú prísľubom pre diabetikov nedosahujúcich cieľové hodnoty LDL-C. Hoci nemáme k dispozícii randomizované klinické štúdie špecificky dizajnované na redukciu KV-rizika v tejto populácii, efekt dokážeme predpokladať zo štúdií s PCSK9-inhibítormi, do ktorých boli diabetici zaradení.
Zameranie sa na manažment aterogénnej dyslipidémie, popri LDL-C, predstavuje pre nás vyššie šance na úspech v redukcii reziduálneho KV-rizika v neustále narastajúcej skupine diabetikov 2. typu.
Doručené do redakcie/ Received: 27. 8. 2017
Prijaté po recenzii/ Accepted: 15. 9. 2017
MUDr. Fábryová Ľubomíra, PhD.
lfabryova@metabolklinik.sk
www.metabolklinik.sk
Zdroje
1. European cardiovascular disease statistics. Dostupné z WWW: <http://www.ehnheart.org/cvd-statistics.html>. [18 Oct 2016].
2. Katsiki N, Tentolouris N, Mikhailidis DP. Dyslipidaemia in type 2 diabetes mellitus: bad for the heart. Curr Opin Cardiol 2017; 32(4): 422–429. Dostupné z DOI: <http://dx.doi.org/10.1097/HCO.0000000000000407>.
3. Anabtawi A, Moriarty PM, Miles JM. Pharmacologic Treatment of Dyslipidemia in Diabetes: A Case for Therapies in Addition to Statins. Curr Cardiol Rep 2017; 19(7): 62. Dostupné z DOI: <http://dx.doi.org/10.1007/s11886–017–0872–8>.
4. Fábryová Ľ. Aterogénna dyslipidémia – nový cieľ v kardiovaskulárnej prevencii. AtheroRev 2016; 1(3): 126–137.
5. Halcox JP, Banegas JR, Roy C et al. Prevalence and treatment of atherogenic dyslipidemia in the primary prevention of cardiovascular disease in Europe: EURIKA, a cross-sectional observational study. BMC Cardiovasc Disord 2017;17(1):160. Dostupné z DOI: <http://dx.doi.org/10.1186/s12872–017–0591–5>.
6. Stone NJ, Robinson JG, Lichtenstein AH et al. ACC/AHA guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines. J Am Coll Cardiol 2014; 63(25 Pt B): 2889–2934. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2013.11.002>. Erratum in J Am Coll Cardiol 2015; 66(24): 2812. J Am Coll Cardiol 2014; 63(25 Pt B): 3024–3025.
7. Lloyd-Jones DM, Morris PB, Ballantyne CM et al. ACC expert consensus decision pathway on the role of non-statin therapies for LDL-cholesterol lowering in the management of atherosclerotic cardiovascular disease risk: a report of the American College of Cardiology Task Force on clinical expert consensus documents. J Am Coll Cardiol 2016; 2016(68): 92–125. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2016.03.519>.
8. [American Diabetes Association]. Standards of medical care in diabetes-2017. 9. Cardiovascular Disease and Risk Management. Diabetes Care 2017; 40(Suppl 1): S75–S87. Dostupné z DOI: <https://doi.org/10.2337/dc17-S012>.
9. Piepoli MF, Hoes AW, Agewall S et al. European guidelines on cardiovascular disease prevention in clinical practice: the sixth joint task force of the European Society of Cardiology and other societies on cardiovascular disease prevention in clinical practice (constituted by representatives of 10 societies and by invited experts). Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J. 2016; 37(29): 2315–2381. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehw106>.
10. Catapano AL, Graham I, De Backer G et al. [Task Force Members; Additional Contributor]. ESC/EAS guidelines for the management of dyslipidaemias. Eur Heart J 2016; 37(39): 2999–3058. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehw272>.
11. Chapman MJ, Blankenberg S, Landmesser U. The year in cardiology 2015: prevention. Eur Heart J 2016; 37(6): 510–519. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehv721>.
12. Collins R, Armitage J, Parish S et al. MRC/BHF Heart Protection Study of cholesterol-lowering with simvastatin in 5963 people with diabetes: a randomised placebo-controlled trial. Lancet 2003; 361(9374): 2005–2016.
13. Colhoun HM, Betteridge DJ, Durrington PN et al. Primary prevention of cardiovascular disease with atorvastatin in type 2 diabetes in the Collaborative Atorvastatin Diabetes Study (CARDS): multicentre randomised placebo-controlled trial. Lancet 2004; 364(9435): 685–696.
14. Kearney PM, Blackwell L, Collins R et al. Efficacy of cholesterol lowering therapy in 18,686 people with diabetes in 14 randomised trials of statins: a meta-analysis. Lancet 2008; 371(9607): 117–125. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(08)60104-X>.
15. Mihaylova B, Emberson J, Blackwell L et al. [Cholesterol Treatment Trialists‘ (CTT) Collaborators]. The effects of lowering LDL cholesterol with statin therapy in people at low risk of vascular disease: meta-analysis of individual data from 27 randomised trials. Lancet 2012; 380(9841): 581–590. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(12)60367–5>.
16. Preiss D, Seshasai SR, Welsh P et al. Risk of incident diabetes with intensive-dose compared with moderate-dose statin therapy: a meta-analysis. Jama 2011; 305(24): 2556–2564. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2011.860>.
17. Livingstone SJ, Looker HC, Akbar T et al. Effect of atorvastatin on glycaemia progression in patients with diabetes: an analysis from the Collaborative Atorvastatin in Diabetes Trial (CARDS). Diabetologia 2016; 59(2): 299–306. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–015–3802–6>.
18. Erqou S, Lee CC, Adler AI. Statins and glycaemic control in individuals with diabetes: a systematic review and meta-analysis. Diabetologia 2014; 57(12): 2444–2452. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–014–3374-x>.
19. Cannon CP, Blazing MA, Braunwald E. Ezetimibe plus a statin after acute coronary syndromes. N Engl J Med 2015; 373(15): 1476–1477. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMc1509363>.
20. Barkas F, Elisaf M, Liberopoulos E et al. Statin therapy with or without ezetimibe and the progression to diabetes. J Clin Lipidol 2016; 10(2): 306–313.Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacl.2015.11.015>.
21. Chapman MJ, Ginsberg HN, Amarenco P et al. [European Atherosclerosis Society Consensus Panel]. Triglyceride-rich lipoproteins and high-density lipoprotein cholesterol in patients at high risk of cardiovascular disease: eveidence and guidance for management. Eur Heart J 2011; 32(11): 1345–1361. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehr112>.
22. Wang D, Liu B, Tao W et al. Fibrates for secondary prevention of cardiovascular disease and stroke. Cochrane Database Syst Rev 2015; (10): CD009580. Dostupné z DOI: <http://dx.doi.org/10.1002/14651858.CD009580.pub2>.
23. Min J, Celine F,Jicheng LV et al. Effects of fibrates on cardiovascular outcomes: a systematic review and meta-analysis. Lancet 2010; 375(9729): 1875–1884. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(10)60656–3>.
24. Sacks FM, Hermans MP, Fioretto P et al. Association between plasma triglycerides and high-density lipoprotein cholesterol and microvascular kidney disease and retinopathy in type 2 diabetes mellitus: a global case-control study in 13 countries. Circulation 2014; 129(9): 999–1008. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.113.002529>.
25. Hermans MP, Fruchart JC, Davignon J et al. Residual Microvascular Risk in Type 2 Diabetes in 2014: Is it Time for a Re-Think? A Perspective from the Residual Risk Reduction Initiative (R3i). J Diabetes Metab 2014; 5(8): 1000413. Dostupné z DOI: <http://dx.doi.org/10.4172/2155–6156.1000413>.
26. Fruchart JC. Selective peroxisome proliferator-activated receptorα modulators (SPPARMα): The next generation of peroxisome proliferator-activated receptor α-agonists. Cardiovasc Diabetol 2013; 12: 82. Dostupné z DOI: <http://dx.doi.org/10.1186/1475–2840–12–82>.
27. Fábryová Ľ. Monoklonálne protilátky proti PCSK9 – nova nádej pre pacientov s vysokým kardiovaskulárnym rizikom. Interná Med 2014; 14(10): 408–416.
28. Gouni-Berthold I, Descamps OS, Fraass U et al. Systematic review of published phase 3 data on anti-PCSK9 monoclonal antibodies in patients with hypercholesterolaemia. Br J Clin Pharmacol 2016; 82(6): 1412–1443. Dostupné z DOI: <http://dx.doi.org/10.1111/bcp.13066>.
29. Sabatine MS, Giugliano RP, Keech AC et al. [FOURIER Steering Committee and Investigators]. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med 2017; 376(18): 1713–1722. <http://dx.doi.org/10.1056/NEJMoa1615664>.
30. Druce I, Abujrad H, Ooi TC. PCSK9 and triglyceride-rich lipoprotein metabolism. J Biomed Res 2015; 29. Dostupné z DOI: <http://dx.doi.org/10.7555/JBR.29.20150052>.
31. Sattar N, Preiss D, Robinson JG et al. Lipid-lowering efficacy of the PCSK9 inhibitor evolocumab (AMG 145) in patients with type 2 diabetes: a meta-analysis of individual patient data. Lancet Diabetes Endocrinol 2016; 4(5): 403–410. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(16)00003–6>.
32. Sattar N, Preiss D, Blom D et al. Evaluation of the one-year efficacy, safety and glycaemic effects of evolocumab (AMG 145) in 4,802 subjects with, at high risk for or at low risk for diabetes mellitus. Presented in the European Association for the Study of Diabetes Stockholm, Sweden, 2015, Sept, 17 Session OP 27.
33. Colhoun HM, Ginsberg HN, Robinson JG et al. No effect of PCSK9 inhibitor alirocumab on the incidence of diabetes in a pooled analysis from 10 ODYSSEY Phase 3 studies. Eur Heart J 2016; 37(39):2981–2989. Dostupné z DOI: <https://doi.org/10.1093/eurheartj/ehw292>.
34. Filippatos TD, Florentin M, Georgoula M et al. Pharmacological management of diabetic dyslipidemia Expert Rev Clin Pharmacol 2017; 10(2): 187–200. Dostupné z DOI: <http://dx.doi.org/10.1080/17512433.2017.1263565>.
Štítky
Diabetologie Endokrinologie Interní lékařstvíČlánek vyšel v časopise
Forum Diabetologicum

2017 Číslo 3
Nejčtenější v tomto čísle
- Rehabilitácia u diabetikov
- Manažment kardiovaskulárneho rizika u diabetikov v svetle aktuálnych odporúčaní
- Diabates mellitus a cerebrovaskulárne ochorenia
- Studie Fourier: Přinesla málo nebo moc? Nebo jen nenaplnila přehnaná očekávání?
